中国抗癌协会
立即下载App期刊|三阴性乳腺癌辅助治疗进展
缺乏雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体2(HER2)表达的乳腺癌被归类为三阴性乳腺癌(triple-negative breast cancer, TNBC),与其他亚型相比,具有侵袭性强、复发早、预后差的特点。来自复旦大学附属肿瘤医院的余科达教授就TNBC辅助治疗进行了系统综述,作者总结了TNBC的传统治疗策略和最新的辅助治疗临床试验,同时评估了TNBC中几个潜在靶点的预后价值和靶向治疗进展。
我们邀请山东省肿瘤医院邱鹏飞教授进行解读。


文章学术观点
NO.1 TNBC辅助治疗
由于TNBC缺乏ER、PR和HER2的表达,化疗仍是TNBC患者的主要辅助治疗方案(表1:不同化疗方案代表性研究)。经典的CMF(环磷酰胺+甲氨蝶呤+氟尿嘧啶)方案是第一个用于乳腺癌患者辅助治疗的联合化疗方案,并在相关研究中观察到对TNBC亚型的显著获益。蒽环类和紫杉类药物的出现进一步降低了早期乳腺癌患者的复发和死亡风险,尤其是淋巴结阳性或TNBC患者。尽管蒽环类药物的远期心脏毒性仍然不容忽视,但目前以蒽环/紫杉类为基础的方案仍然是TNBC辅助治疗的标准方案。
卡培他滨作为口服的氟尿嘧啶前药,目前常用于与其他化疗药物(如蒽环/紫杉类化疗)联合使用:FinXX研究首次表明在传统辅助化疗方案中增加卡培他滨可改善TNBC患者的生存预后;CBCSG-010试验进一步证实了在多西他赛、表柔比星和环磷酰胺的辅助化疗方案中加入卡培他滨可改善TNBC患者5年的无病生存率(DFS),但总生存(OS)无显著差异;SYSUCC-001研究提示在早期TNBC标准治疗后使用低剂量、高频率卡培他滨维持治疗可以显著改善DFS。另外,铂类药物可以提高TNBC患者新辅助治疗病理完全缓解(pCR),但是否改善预后仍有待证实;PATTERN试验显示TNBC辅助治疗中PCb方案相比传统CEF-T方案可显著改善5年DFS(但OS无差异)。因此,卡培他滨或铂类药物的加入可能为TNBC患者提供额外获益,但药物的不良反应仍然不容忽视。
与标准化疗方案相比,剂量密集型化疗方案可以改善乳腺癌患者(特别是高危患者)的预后,NCCN指南将含蒽环紫杉类的剂量密集方案作为HER2阴性乳腺癌新辅助/辅助化疗的优选方案之一。然而,剂量密度的增加与更严重的化疗相关毒性和不良事件显著相关,建议在剂量密集化疗期间密切监测副作用。
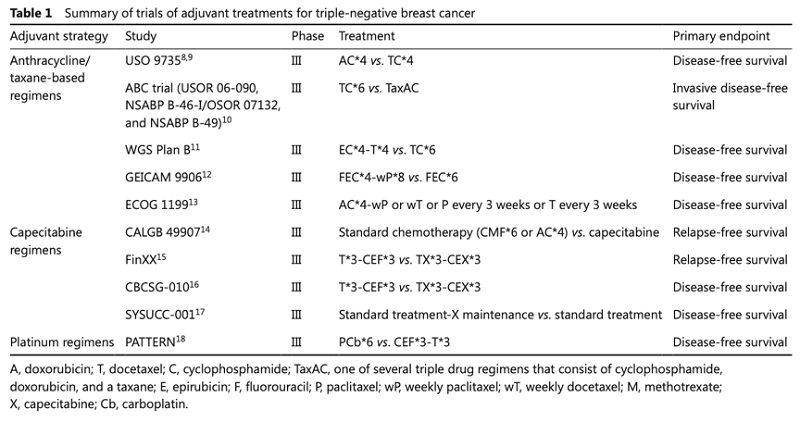
表1:不同化疗方案代表性研究
NO.2 TNBC分子亚型
TNBC作为一种高度异质性的亚型,可以进一步分为几个分子亚型,这些亚型具有相似的基因组或转录特征,并可能受益于特定的治疗策略。目前,TNBC亚型通常以科学研究为目的,尚未广泛用于临床实践。Lehmann等将TNBC细分为4个不同的亚型:2种基底样(BL1和BL2)、间质型(M)和管腔雄激素受体(LAR)亚型。复旦大学附属肿瘤医院邵志敏和江一舟等学者使用多组学分析从基因组和转录组学的角度将中国TNBC患者分为4个亚型:免疫调节型(IM)、管腔雄激素受体型(LAR)、基底样免疫抑制型(BLIS)、间质型(MES)。随后,该研究团队开展FUTURE研究探索难治性转移性TNBC的精准治疗,初步结果显示出基于复旦分型靶向治疗的获益。
NO.3 TNBC 潜在靶点和治疗策略
随着测序技术的发展和相关细胞通路的探索,TNBC不再是传统认知中的单一类型,许多临床试验正在研究TNBC的有效治疗靶点(表2:TNBC潜在通路、预后因素和治疗药物)。BRCA1/2突变的肿瘤通常无法通过同源重组修复双链断裂,因此这部分患者可能对DNA损伤化合物(如铂类药物)和PARP抑制剂更敏感;BRCA在指导乳腺癌铂类药物应用方面目前仍存在争议,但PARP抑制剂在BRCA1/2突变乳腺癌辅助治疗和解救治疗的有效性已被OlympiA、OlympiAD和EMBRACA等大型临床研究所证实。
EGFR抑制剂和VEGF抑制剂在既往研究中显示的效果有限,并不作为TNBC治疗的首选策略。PI3K/AKT/mTOR通路是TNBC治疗的潜在靶点,尤其是对于携带PIK3CA、AKT或PTEN基因突变的患者,相关药物的有效性和不良反应有待进一步验证。抗雄激素治疗可能使雄激素受体(AR)表达的TNBC患者获益,但其机制尚不明确,需要进一步研究证实AR在TNBC中的指导意义。
免疫治疗作为近年来的热门研究领域,相关研究已经显示出其在TNBC新辅助治疗中的有效性,同时TIL和PD-L1表达可以显著影响TNBC患者的pCR;但其在辅助治疗方面仍缺乏强有力的证据,有待进一步验证才能将其纳入TNBC患者的标准辅助治疗。

表2:TNBC潜在通路、预后因素和治疗药物
专家解读
TNBC是预后较差的分子亚型,由于缺乏治疗靶点,化疗仍然是目前主要的治疗手段,这篇综述全面总结了TNBC辅助治疗策略、分子亚型、潜在靶点的预后价值和靶向治疗进展。精准医学时代,TNBC个体化治疗已经初见成效,但临床上仍然存在一系列问题有待深入研究:
乱花渐欲迷人眼—辅助强化如何精准决策
近年来TNBC治疗模式的转变和循证医学证据的积累对早期TNBC治疗决策提出了新的挑战。尽管以蒽环/紫杉类为基础的方案仍是早期TNBC辅助治疗的标准方案,但已经不能包打天下。CBCSG-010、SYSUCC-001和PATTERN等研究相继证实卡培他滨和卡铂等老牌药物的加盟可以改善TNBC的预后;OlympiA等研究也使PARP抑制剂等新型药物在辅助强化阶段展露峥嵘;EBCTCG荟萃分析则显示出剂量密集型相比于标准化疗方案可以降低乳腺癌复发死亡风险。那么对于早期高危TNBC究竟是在蒽环紫衫基础上加用卡培他滨,还是选择剂量密集方案?如果伴有BRCA1/2突变,在选择PARP抑制剂的基础上是否兼顾上述其他强化治疗?几种强化治疗又是如何排兵布阵?不得而知。同时,不论是剂量密集型方案,还是卡培他滨、免疫制剂和PARP抑制剂等药物的加入,在增加疗效的同时也伴随更多的不良反应。因此,在临床实践中如何实现早期TNBC治疗决策的“优化组合”,仍然是肿瘤医生所面临的挑战之一。
远上寒山石径斜—新辅助治疗pCR与生存获益
目前新辅助治疗已经成为TNBC的优选治疗模式,新辅助治疗方案也在不断探索和优化,铂类药物、免疫检查点抑制剂和PARP抑制剂等药物的加入也使TNBC的pCR率更上层楼。一方面,我们在努力提高pCR比例的同时,希望探索出更多诸如PD-L1、CD8、27基因评分等疗效预测工具,以实现系统治疗的升/降阶梯。另一方面,我们期待pCR可以转化成为最终的生存获益,但同时也看到新辅助治疗对于外科手术乃至放射治疗的影响;尽管目前KEYNOTE-522、GeparSixto和GeparNUEVO等新辅助临床研究的结果不一而足,但在追求最终生存获益的漫漫征途上,pCR对于局部区域降阶梯的贡献也足以值得欣喜。
拨云见日终有时—分型而治未来可期
随着基因检测技术的迅猛发展和靶向药物不断涌现,尽管当下化疗仍然是TNBC辅助治疗的主流,但个体化和精准化在TNBC中已经初见成效。复旦大学附属肿瘤医院团队基于中国人群绘制出TNBC多组学图谱,并据此提出TNBC复旦分型,然后针对每个亚型鉴定一些潜在的治疗靶点,FUTURE研究已使既往难治型TNBC患者初见曙光。TNBC的未来是“分型而治”,免疫治疗、PARP抑制剂、ADC药物、PI3K-AKT-mTOR抑制剂等靶向治疗有望使更多的早期TNBC走向治愈。

主任医师,医学博士,博士后,硕士生导师。山东省肿瘤医院乳腺外科一病区副主任。齐鲁卫生与健康杰出青年人才,山东省高层次人才,山东省高等学校青创人才团队核心成员,中华医学会肿瘤学分会乳腺肿瘤青年学组委员,中国抗癌协会乳腺癌专业委员会青年专家,中国抗癌协会国际医疗交流分会委员,山东省抗癌协会肿瘤免疫与免疫治疗学分会委员。Cancer Biology & Medicine 青年编委。主持国家自然科学基金项目2项, 第一/通讯作者在Lancet Oncology等学术期刊发表论文30余篇。