中国抗癌协会
立即下载App中国科研之声 | 恩沙替尼一线治疗研究在JAMA Oncology正式发表,中国PI吴一龙教授深入解读eXalt3 研究亮点

编者按
【中国科研之声】2021年9月2日,全球顶尖学术期刊JAMA Oncology在线发布了由广东省人民医院吴一龙教授担任中国PI的全球多中心随机开放的临床研究——克唑替尼对比恩沙替尼未经治疗人群(一线)eXalt3 研究结果(数据截止日期2020年7月1日),文章题目为:Ensartinib vs Crizotinib for Patients With Anaplastic Lymphoma Kinase−Positive Non–Small Cell Lung Cancer A Randomized Clinical Trial,影响因子(IF)为31.777。

eXalt3 研究提示,恩沙替尼一线治疗数据扎实,中国自主研发的第一个ALK-TKI恩沙替尼将成为ALK阳性NSCLC患者一线治疗的全新选择。
【研究者简介】

吴一龙 教授
肿瘤学教授,博士生导师
IASLC杰出科学奖获得者
2018-2020年临床医学领域全球高被引学家
2020年世界肺癌大会(WCLC )主席
广东省人民医院(GDPH)终身主任
广东省肺癌研究所(GLCI)名誉所长
广东省肺癌转化医学重点实验室主任
吴阶平基金会肿瘤医学部会长
中国医师协会精准医学专委会副主任委员
广东省临床试验协会(GACT)会长
中国胸部肿瘤研究协作组(CTONG)主席
广东省医学会肺部肿瘤学会主任委员
中国临床肿瘤学会前任理事长,现指导委员会主任委员
【研究者说】
eXalt3研究是一项全球开放多中心随机对照Ⅲ期临床研究,全球牵头PI为Leora Horn教授,中国牵头PI是广东省人民医院吴一龙教授。医悦汇【中国科研之声】栏目特邀该研究中国PI吴一龙教授作为访谈嘉宾,对恩沙替尼一线治疗研究数据及研究结果进行深入解读。
医悦汇:eXalt 3 研究设计的背景和创新点有哪些?
吴一龙教授:ALK通路是肺癌精准治疗的重要组成部分,肺癌精准治疗的特点是必须先发现基因突变靶点,然后根据基因突变靶点设计靶向药物进行临床治疗。研究发现,ALK基因融合正是一个重要的驱动基因,科研工作者也根据ALK驱动基因设计了一系列的靶向药物。
从2010年开始,我们先找到了ALK靶点,并研发出了一代ALK-TKI克唑替尼,其在ALK阳性NSCLC治疗中显示出非常好的效果,中位PFS达到了11个月,相比化疗的6个月,显著改善了患者的获益,由此克唑替尼成为ALK阳性NSCLC标准的一线治疗策略。
继克唑替尼之后,如果想在ALK通路上取得突破,必须与标准一线治疗克唑替尼进行头对头的比较,唯有疗效超过克唑替尼才能进入临床视野。后续新的ALK-TKI如色瑞替尼、阿来替尼、劳拉替尼及布加替尼等陆续诞生,并在临床研究和治疗中取得了非常好的成绩。基于此,在这些药物之后,要想研发出更好的新药物,不仅要考虑到赢过基本标准的克唑替尼,同时也要考虑到相比这么多的同类产品,它的优势在什么地方?在这样一个背景下,eXalt 3 研究如何更好的开展就需要考虑更多因素。
实际上,在eXalt 3 研究上有两方面的创新:①改良了ITT人群。尽管现在很多医院都可以进行ALK基因检测,但基因检测的质量还存在参差不齐的现象,因此研究加入了改良的ITT人群,就是把所有标本放到同一个中心实验室进行检测,根据中心实验室的阳性结果作为入组标准之一。②非常注重药物对脑转移的治疗效果。在入组时,我们有意识的选择比较多的脑转移患者进入研究,以期更好评估恩沙替尼对脑转移治疗的效果。
医悦汇:目前发表的数据截止于2020年7月1日,您认为PFS数据后续还有无可能继续延长?
吴一龙教授:ITT人群PFS是否成熟取决于患者的事件率是否达到要求,如果事件率已经达到50%以上,一般而言PFS不会有很大的改变。
这次报道结果显示,ITT人群中,50%患者已经达到事件,因此ITT人群的PFS延长可能性比较小,但是数字可能会有略微变化。如果是改良的ITT人群,目前达到事件的患者还没有一半,所以改良ITT人群 的PFS还会发生改变,后续可能会更长。
医悦汇:恩沙替尼与现有ALK-TKI相比有哪些不同?
吴一龙教授:以今天的眼光来评价ALK-TKI的优劣,有以下三个标准:①ALK抑制剂是否能够通过血脑屏障。药物能够通过血脑屏障就意味着出现脑转移的比例会大大下降。②安全性。患者服用药物时间越来越长,药物的安全性就越重要,必须保证药物长时间服用所伴随的不良反应在一定范围内是可控的。③能否克服已知的耐药机制。如果符合以上三点要求和标准,我们认为这类药物就是好药。
从现有的研究数据中我们看到,恩沙替尼在脑转移的控制力是传统克唑替尼的三倍,对脑转移的控制力可以达到很好的高度。同时,安全性非常高,目前其在不良反应风险上并没有高于其他ALK抑制剂。此外,恩沙替尼对一些常见的耐药突变位点也有一定的抑制作用。综合来看,恩沙替尼有非常鲜明的特色,相信恩沙替尼的上市会给我们提供非常好的治疗选择。
医悦汇:结合eXalt 3研究,您如何看待未来恩沙替尼一线应用的前景?
吴一龙教授:根据eXalt 3研究结果,恩沙替尼在中国获批一线治疗适应证上市的可能性是极大的。目前,在中国上市的ALK抑制剂相比在全球范围内可使用的ALK-TKI更少,如布加替尼和劳拉替尼在中国还没有上市,所以恩沙替尼在中国的一线适应证获批所面临的竞争程度相比全球上市会少些。实际上,恩沙替尼的二线治疗适应证在中国已经获批上市,此次在中国的上市申请只是增加一线治疗适应证,难度相比也会小一点。总之,凭借恩沙替尼在一线治疗研究中的优越表现,其获批一线治疗上市的可能性非常大。
另外,恩沙替尼上市后将为中国肺癌患者提供了更多新的治疗选择。作为中国制药企业开发的原研靶向药物,相信其在价格上也会有一定的优势,这对患者治疗而言也会有更好的可接受性。
医悦汇:eXalt 3 研究设计中有ITT人群和mITT人群,设计mITT人群的意义何在?
吴一龙教授:我们知道不同地方检测同类标本,质量控制非常重要,但显然每个医院质控标准不尽相同,这可能会导致检测结果不会是非常均一和同质化的。但也要看到,ALK检测已经成为各家医院的基本检测方法之一,因此eXalt3的意向人群,采用的是各个site只要检测出ALK融合就可以入组。而mITT,指的是通过中心实验室检测确认是ALK融合才计算为意向人群,因此也称为改良的意向人群。
我们用mITT作为一个标准,就是通过中心实验室把所有检测的质量都控制在同一水平上。我们可以看到,目前研究中mITT人群的中位PFS还没有达到,意味着对精准治疗中检测质量的控制非常重要,也就是说高水平、一致化的检测中心诊断的ALK阳性患者后续临床治疗的获益会更大。如果入组时依靠各个实验室做出来的检测结果,则有可能会出现假阴性或者假阳性的结果,尤其一旦入组假阳性患者,一定会影响研究数据的准确性。
此外,eXalt 3研究也给我们提出了一个新的问题——未来如何在检测方面做到同质化来保证高质量的检出,这对患者的精准治疗是至关重要的。
医悦汇:eXalt 3 研究此次发表在JAMA Oncology对国内创新药企或者说对ALK-TKI治疗领域发展有哪些深远的影响?
吴一龙教授:我个人认为,文章的质量并不在于发表在什么杂志上,每个杂志的评判标准是不同的。我认为发表在20分以上或者30分以上的文章质量应该是处在同一水平的。如果将医学杂志分档,那么能够发表在NEJM、JAMA、The Lancet等杂志主刊显然是第一梯队,发表在这些重要杂志子刊则属于第二梯队。恩沙替尼的一线治疗研究能够发表在第二梯队的杂志足以说明研究质量是非常高的。
希望中国本土制药企业在把临床试验交给研究者设计时,一定不要照搬以往类似的临床试验,务必要结合研究者临床实践的考量,让研究设计更具有创新性,这样才能发表在更高影响力的杂志上。这也是恩沙替尼一线研究给我们的启示。
【eXalt3 研究简介】
eXalt3 研究旨在评估恩沙替尼对比克唑替尼对未经过治疗的(一线)携带ALK阳性NSCLC患者治疗的疗效和安全性。其研究结果首次公布于2020 WCLC Presidential Symposium会议;并于2021年1月28日在2020 WCLC公布了eXalt3研究随访更新数据。本次在JAMA Oncology发布的eXalt3研究数据截止日期为2020年7月1日。

研究设计
eXalt 3 研究全球总计入组290名患者,其中中国入组140名患者,分为试验组和对照组。试验组为恩沙替尼225mg QD方案,直至疾病进展;对照组为克唑替尼250mg BID方案,直至疾病进展,两组之间不允许交叉。主要研究终点为BIRC评估的ITT人群的mPFS;关键次要研究终点为OS, ORR/DOR(overall and brain), TTF in the brain, QOL(EORTC, LCSS)。
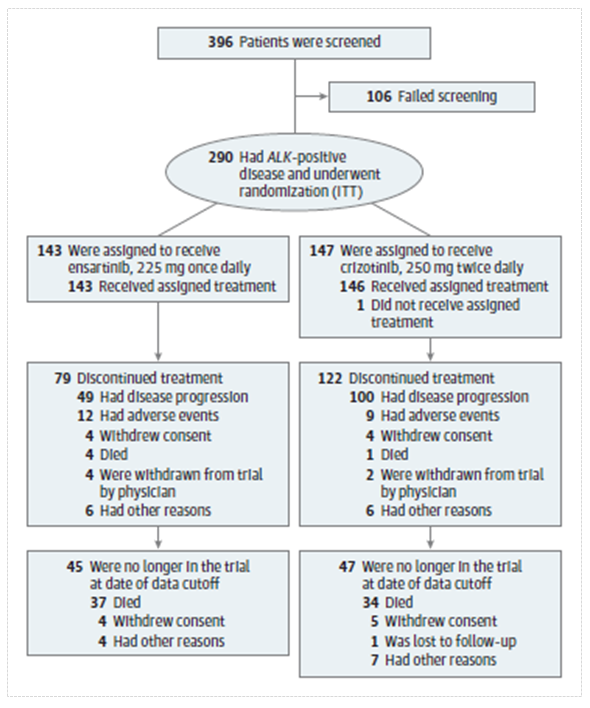
研究结果
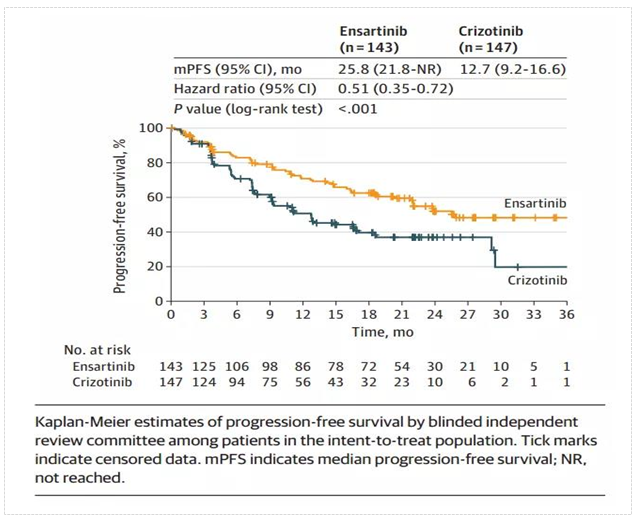
PFS和OS数据 根据2020年7月1日的数据库锁定日期,于2020年8月8日进行了中期分析:在ITT人群中,恩沙替尼的中位无进展生存期(mPFS)为25.8个月,克唑替尼的中位无进展生存期(mPFS)为12.7个月;HR为0.51(95%CI为0.35-0.72;P<0.001)。
在改良的ITT人群(中心确诊的ALK+NSCLC患者)中,恩沙替尼组PFS中位数未达到,而克唑替尼组为12.7个月;HR, 0.45;(95% CI为0.30-0.66;P<0.001)。在改良的ITT人群中,恩沙替尼组和克唑替尼组均未达到中位总生存率(OS)。12个月时脑转移发生率恩沙替尼组为4.2%,对照组克唑替尼组为23.9%,HR为0.32(95%CI为0.16-0.63;P=0.001)。
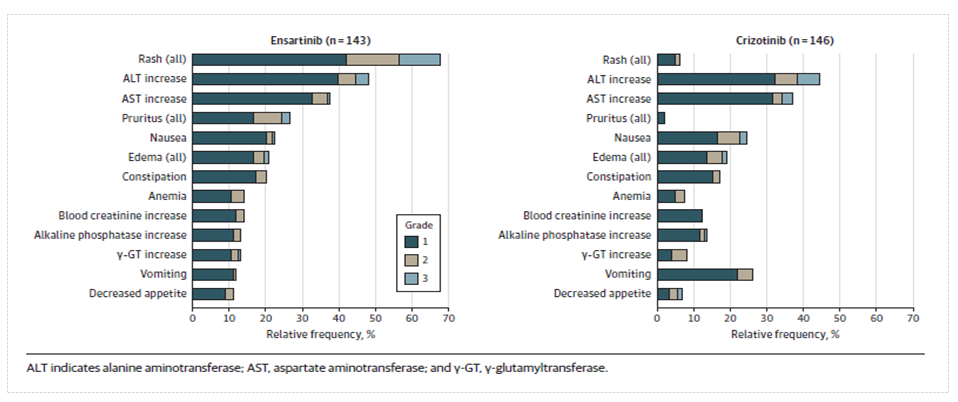
安全性数据 研究展现出恩沙替尼具有良好的耐受性,常见不良反应为一过性皮疹,相比较内脏及血液毒性,具有易发现易处理的特点。
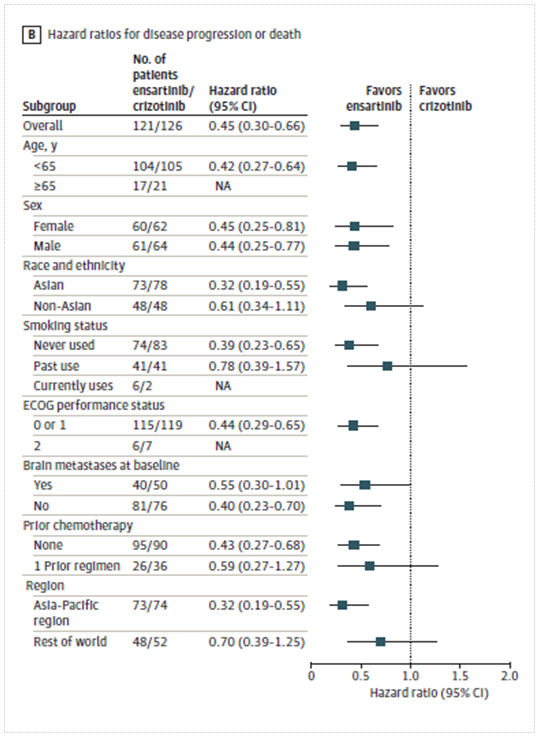
【研究意义】
非小细胞肺癌(NSCLC)在肺癌中的占比约85%,其中5%~7%的NSCLC患者会发生ALK重排。恩沙替尼是一种有效的新一代ALK-TKI,在美国及中国一二期临床研究中均表现出确切的疗效和良好的安全性。鉴于恩沙替尼在国内注册二期临床研究中的优异表现,国家药监局(NMPA)于2020年11月19日核准签发了《药品注册证书》,标志着恩沙替尼正式在中国获批上市。成为中国第一个用于治疗ALK阳性NSCLC的国产1类新药。
此次JAMA Oncology发表的恩沙替尼一线研究数据再一次让中国自主原研靶向药在世界舞台发出中国科研好声音,eXalt3研究数据的出炉也为恩沙替尼在中国一线治疗适应证获批以及全球上市奠定了坚实的基础。截止2021年8月恩沙替尼累计发表SCI文章共15篇,影响因子累计138.613。
【关于“中国科研之声”】
“中国科研之声”栏目由医悦汇设立,发布中国肿瘤科研工作者的研究成果,旨在为中国肿瘤领域科研工作者提供一个学术成果展示、交流和分享的平台,以期共同学习,共同进步。
投稿邮箱:yiyuehuioncology@163.com
投稿微信:
18412041410