中国抗癌协会
立即下载App盘点2020 | 张清媛教授:2020年度HR+乳腺癌内分泌治疗领域进展

一个年度的盘点,也是下一个年度的起点
酸甜交错的2020离我们远去
充满期盼的2021向我们走来
【医悦汇】保持传统
诚邀肿瘤领域大咖
推出新年特辑【年度盘点】
总结盘点2020年度肿瘤学科进展
以字为媒,以言为镜
汇集和解读属于肿瘤学者的2020
第19期

哈尔滨医科大学附属肿瘤医院 张清媛教授
2020年度HR+乳腺癌内分泌治疗领域进展
特邀专家


盘点2020年度HR+乳腺癌内分泌治疗领域进展
世界卫生组织国际癌症研究机构(IARC)发布2020年最新癌症负担数据显示,全球乳腺癌新发病例高达226万例,超过肺癌成为全球第一大癌[1]。2020年是极不平凡的一年,新冠疫情对全球格局产生深远影响,但并未阻挡乳腺肿瘤学者开拓进取的热情。值此新年伊始,我们就2020年度HR阳性乳腺癌领域内分泌治疗热点研究进行如下梳理。
1 新辅助内分泌治疗药物优化探索
新辅助内分泌加入Fulvestrant:ALTERNATE研究
ALTERNATE研究[2]旨在比较Fulvestrant单药或联合阿那曲唑对比阿那曲唑单药是否提高内分泌治疗敏感性疾病率(ESDR);同时评估不同用药策略治疗前后及手术时Ki-67水平。如果第4周或第12周Ki-67>10% 则认为对内分泌治疗耐药,需接受新辅助化疗。结果显示三组患者在ESDR率和降低Ki-67水平方面未见显著差异。补救性NCT对NET后Ki-67>10%耐药患者pCR率只有4.8%,大多数患者在NCT后仅有RCB-II和RCB-III的疗效,提示存在较高复发风险。但该研究仅1/3患者使用AC-taxol强效新辅助化疗方案,这可能也影响了pCR。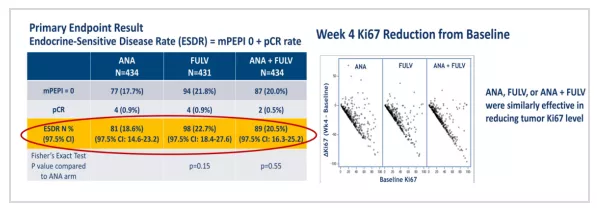
新辅助内分泌联合CDK4/6抑制剂——FELINE研究
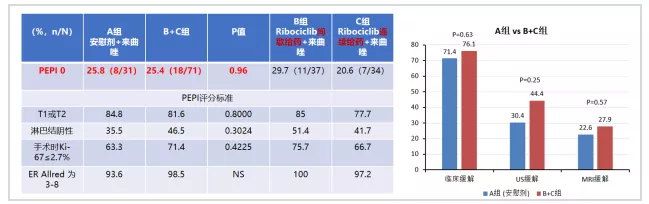
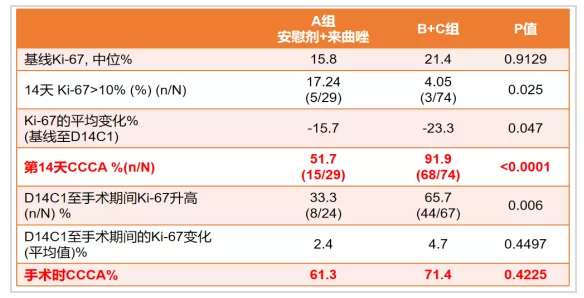
研究入组绝经后、肿瘤>2cm或淋巴结阳性ER+/HER2-患者,分别接受六周期来曲唑+安慰剂、来曲唑+Ribociclib 400mg连续给药或来曲唑+Ribociclib 600mg间歇给药新辅助治疗。评估治疗前、D14C1及手术时Ki-67状态。主要研究终点为术前内分泌治疗预后指数评分(PEPI)0分患者所占比例,次要终点为D14C1完全细胞周期停滞率(CCCA,即:Ki-67≤2.7%)及缓解率。结果显示:来曲唑+安慰剂及Ribociclib+来曲唑组间PEPI 0分患者比例(25.8% vs 25.4%,P=0.96)及缓解率(P=0.63)未见显著差异。来曲唑+安慰剂组与Ribociclib+来曲唑组D14C1达CCCA者分别占51.7%和91.9%,组间差异显著。然而手术时联合治疗组CCCA比例降至71.4%,组间无显著差异[3]。Ribociclib+来曲唑在D14C1对Ki-67的早期抑制未能持续到手术时,可能由于治疗过程中出现Ribociclib获得性耐药。
Ribociclib+来曲唑 vs AC-T化疗——CORALLEEN研究
研究入组绝经后Ⅰ-ⅢA期,肿瘤大小≥2cm ,Luminal B型乳腺癌,主要终点为评估手术时ROR评分低的疾病比例。化疗组和RIB + LET 组在ROR低分组无差异,但Ribociclib联合来曲唑组pCR,RCB 0-1率和临床反应率都低于化疗,但内分泌治疗组毒性相对较低[4]。基于CORALLEEN研究目前仍是初步结果,这种治疗组合作为高危LuminalB型乳腺癌化疗的替代治疗效需进一步证实。
2 辅助内分泌治疗“加减法”
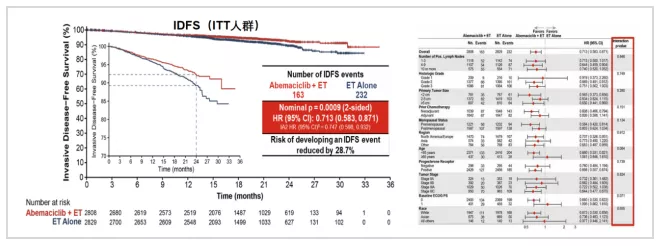
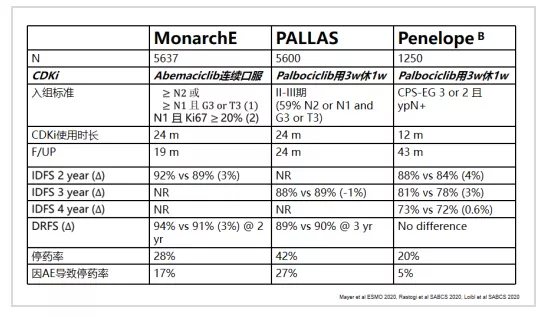
加法——高危患者辅助内分泌联合CDK4/6imonarchE研究[5]入组≥4 枚阳性腋窝淋巴结或1-3 枚阳性ALN以及至少符合以下情况之一:肿瘤≥5 cm;组织学分级3级或Ki-67 ≥20% 高危早期乳腺癌患者,比较Abemaciclib联合标准辅助内分泌治疗与单纯标准辅助内分泌疗效,主要研究终点为无浸润性疾病生存期。2020 ESMO会议公布结果显示,Abemaciclib+ET组与单用ET组2年IDFS率分别为92.2%和88.7%,绝对改善为3.5%,各预设亚组均呈现一致显著获益。Abemaciclib联合内分泌治疗显著降低远处复发风险,特别是骨、肝等部位,且耐受性良好。2020SABCS monarchE研究结果更新:随访至19.1个月,有更好的统计学意义和IDFS的改善,两组2年IDFS率相差3.0%,支持所有亚组获益一致。在Ki-67 高表达患者,2年IDFS率及2年DRFS率在Abemaciclib联合ET组改善更佳[6]。
然而Palbociclib联合辅助内分泌治疗的PALLAS III期研究并未取得阳性结果。研究入组术后II-III期HR+/HER2-乳腺癌,包括淋巴结阳性和阴性患者[7],相比monarchE研究入组了一些相对低危的患者;另一项Palbociclib联合内分泌治疗的PENELOPE-B研究,入组新辅助化疗术后non-PCR患者,中位随访42.8个月也未取得阳性结果。NACT后高复发风险患者加用1年Palbociclib并不能改善iDFS[8]。三项CDK4/6i辅助治疗各研究结果不同,差异可能由于人群筛选、药物本身特点、耐受性、用药时长等。
减法——基因检测助力辅助治疗降阶梯
21基因检测指导腋窝淋巴结阴性低风险乳腺癌临床价值已被认可。对于1-3枚淋巴结阳性的患者,能否根据21基因检测判断HR+/HER2-低危患者豁免化疗也是辅助治疗需要研究的重点。2020年SABCS会议报道RxPONDER研究中期结果显示:1-3枚LN阳性,RS 0-25绝经后患者不能从化疗中获益,辅助阶段不使用化疗可能是安全的;RS 0-25绝经前妇女,化疗降低了46%的IDFS事件,绝经前妇女可能在化疗中显著获益[9]。
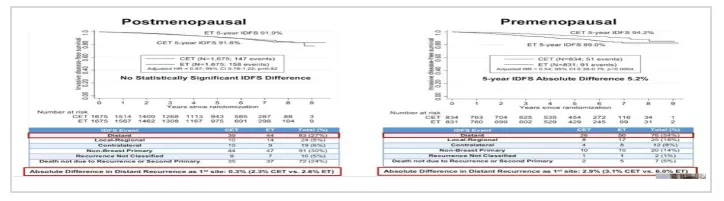 2020年ASCO大会报道MINDACT试验随访8.7年结果,该研究将基因评估和临床评估不一致患者,随机分为单纯内分泌治疗以及CT联合内分泌治疗。其中C-High/G-Low组中未化疗患者5年DMFS为95.1%,化疗与未化疗组5年DMFS差异是0.9%年,8年DMFS差异则增大为2.6%。探索性亚组分析显示对于绝经后患者,化疗基本未带来获益,豁免化疗具有可行性;而<50岁非绝经患者,化疗获益高达5%,豁免化疗需慎重。而C-low患者无论G-low或G-high5年和8年DMFS率下限均在92%以上,提示此类患者或许不必盲目进行基因检测;此类患者化疗获益尚不显著,或许可以免除化疗[10]。
2020年ASCO大会报道MINDACT试验随访8.7年结果,该研究将基因评估和临床评估不一致患者,随机分为单纯内分泌治疗以及CT联合内分泌治疗。其中C-High/G-Low组中未化疗患者5年DMFS为95.1%,化疗与未化疗组5年DMFS差异是0.9%年,8年DMFS差异则增大为2.6%。探索性亚组分析显示对于绝经后患者,化疗基本未带来获益,豁免化疗具有可行性;而<50岁非绝经患者,化疗获益高达5%,豁免化疗需慎重。而C-low患者无论G-low或G-high5年和8年DMFS率下限均在92%以上,提示此类患者或许不必盲目进行基因检测;此类患者化疗获益尚不显著,或许可以免除化疗[10]。
3
晚期HR+ BC:CDK4/6抑制剂最佳一线联合搭档探索
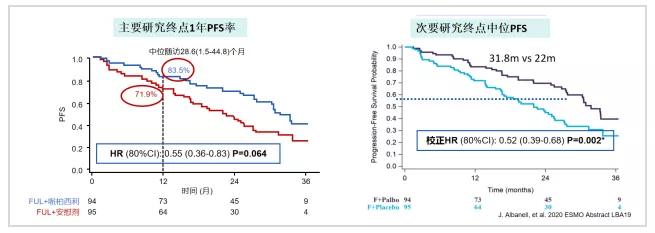
FLIPPER研究进一步补充了氟维司群作为CDK4/6抑制剂一线联合搭档的循证医学证据。研究纳入绝经后初诊IV期或完成≥5年辅助内分泌治疗后超过12个月复发的内分泌治疗敏感的mBC患者,比较氟维司群+Palbociclib和氟维司群+安慰剂组疗效。中位随访28.6个月,主要终点1年PFS率、mPFS及ORR方面都取得了氟维司群联合CDK4/6抑制剂显著优势[11]。
2020年ASCO公布PARSIFAL研究纳入既往内分泌治疗敏感且晚期阶段未接受过治疗患者,分别接受Palbociclib+氟维司群或Palbociclib+来曲唑治疗。结果CDK4/6i 联合Ful未显示比联合AI 有优势,但非劣效性界值未能达到预设,孰优孰劣尚无定论[12]。最终治疗决策必须平衡患者和临床医生的偏好以及后续治疗策略。
4 精准医学助力晚期HR+乳腺癌联合治疗
ESR1突变参与内分泌耐药,PADA-1研究旨在通过检测血清游离DNA,探索基线ESR1突变及治疗后ESR1突变与一线PAL+AI疗效及进展后选择的相关性。结果显示ESR1突变与一线AI为基础治疗后短的PFS相关,支持行ESR1突变筛查。同时发现33例初诊时存在ESR1突变患者有23例在治疗1个月后出现“ESR1突变清除”,且清除患者预后较好,说明CDK4/6i具有逆转内分泌耐药的作用[13]。SOLAR-1研究入组AI治疗进展患者,对于PIK3CA突变队列,Alpelisib+氟维司群与安慰剂+氟维司群组mPFS分别为11.0个月和5.7个月;内分泌耐药患者Alpelisib+氟维司群组mPFS为9.4个月,安慰剂+氟维司群组为4.2个月。Alpelisib获批与氟维司群联合治疗绝经后晚期HR+HER2-PIK3CA突变乳腺癌。2020年ESMO公布SOLAR-1次要终点OS结果,Alpelisib+氟维司群和安慰剂+氟维司群mOS分别为39.3个月和31.4个月,虽未达到统计学差异,但mOS延长了7.9个月。亚组分析显示,对于有肺/肝转移或血浆ctDNA中检测出PIK3CA突变患者,接受Alpelisib+氟维司群有OS改善[14]。Alpelisib的加入推迟了PIK3CA突变队列停药后再次启动首次化疗时间,进一步支持了主要研究终点PFS的获益结果。

2020年ASCO大会公布BYLieve研究队列A(先前接受CDK4/6i联合AI组)研究结果,中位随访11.7个月,Alpelisib+氟维司群队列在6个月时无疾病进展患者比例为50.4%,mPFS为7.3个月。2020年SABCS大会上报告队列B(先前接受CDK4/6i联合Fulvestrant组)研究结果,中位随访15个月,Alpelisib+来曲唑队列在6个月时无疾病进展患者比例为45.8%,mPFS为5.7个月。队列A、B均达到预-设主要研究终点,提示对于HR阳性HER2阴性伴PIK3CA突变晚期乳腺癌患者,一线CDK4/6抑制剂治疗进展后,PI3K抑制剂联合内分泌治疗有效。Alpelisib严重不良反应率低,且不良事件可控。与真实世界治疗的匹配分析表明,Alpelisib +氟维司群对比标准治疗PFS获益更显著,且安全性良好。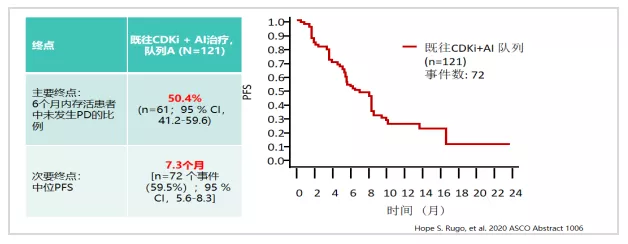
总结
暮去朝来,时光荏苒。过去一年乳腺癌内分泌治疗取得重要进展,也面临新的挑战。探索新辅助内分泌治疗合适的药物和给药方式,临床病理特征联合基因工具筛选辅助内分泌治疗患者豁免化疗以及精准医疗助力晚期治疗排兵布阵,克服逆转内分泌耐药仍是未来探索的方向,期待更多研究数据为临床决策提供支持。参考文献
[1] Latest global cancer data: Cancer burden rises to 19.3 million new cases and 10.0 million cancer deaths in 2020. Retrieved Dec 16, 2020, from https://www.iarc.fr/faq/latest-global-cancer-data-2020-qa/
[2] Qamar J. Khan, et al. Validation of a predictive model for potential response to neoadjuvant endocrine therapy (NET) in postmenopausal women with clinical stage II or III estrogen receptor positive (ER+) and HER2 negative (HER2-) breast cancer (BC): An ALTERNATE trial analysis (Alliance A011106) .2020 SABCS.
[3] Qamar J. Khan, et al.Letrozole + ribociclib versus letrozole + placebo as neoadjuvant therapy for ER+ breast cancer (FELINE trial).2020 ASCO.
[4] Prat A,Saura C,Pascual T, et al. Ribociclib plus letrozole versus chemotherapy for postmenopausal women with hormone receptor-positive, HER2-negative, luminal B breast cancer (CORALLEEN): an open-label, multicentre, randomised, phase 2 trial.[J] .Lancet Oncol, 2020, 21(1): 33-43.
[5] Johnston SRD,Harbeck N,Hegg R et al. Abemaciclib Combined With Endocrine Therapy for the Adjuvant Treatment of HR+, HER2-, Node-Positive, High-Risk, Early Breast Cancer (monarchE).[J] .J Clin Oncol, 2020, 38:(34) 3987-3998.
[6] O’Shaughnessy J, Johnston SRD, Harbeck N, et al. Primary outcome analysis of invasive disease-free survival for monarchE: abemaciclib combined with adjuvant endocrine therapy for high-risk early breast cancer. SABCS 2020.Abstract GS1-01.
[7] Mayer EL, et al. 2020 ESMO Abstract LBA12.
[8] Loibl S, Marmé F, Martin M, et al. Phase III study of palbociclib combined with endocrine therapy (ET) in patients with hormone-receptor-positive (HR+), HER2-negative primary breast cancer and with high relapse risk after neoadjuvant chemotherapy (NACT): First results from PENELOPE-B. SABCS 2020. Abstract GS1-02.
[9] Kalinsky K, et al. 2020 SABCS Abstract GS3-00
[10]Fatima C,et al. Long-term MINDACT Results Affirm Excellent Prognosis for Clinically and Genetically Low-Risk Early Breast Cancer.[J] .Oncologist, 2021, doi:10.1002/onco.13666
[11]J. Albanell, et al. 2020 ESMO Abstract LBA19
[12]Antonio Loombart-Cussac, et al. 2020 ASCO Abstract 1007
[13]Nikhil W,et al. 2020 ASCO
[14]Fabrice A, et al. 2020 ESMO Abstract LBA18
[15]Hope SR, et al.Alpelisib (ALP) + fulvestrant (FUL) in patients (pts) with PIK3CA-mutated (mut) hormone receptor-positive (HR+), human epidermal growth factor receptor 2-negative (HER2–) advanced breast cancer (ABC) previously treated with cyclin-dependent kinase 4/6 inhibitor (CDKi) + aromatase inhibitor (AI): BYLieve study results. 2020 ASCO Abstract 1006