中国抗癌协会
立即下载App盘点2020 | 程颖教授:2020年度小细胞肺癌内科治疗领域进展

一个年度的盘点,也是下一个年度的起点
酸甜交错的2020离我们远去
充满期盼的2021向我们走来
【医悦汇】保持传统
诚邀肿瘤领域大咖
推出新年特辑【年度盘点】
总结盘点2020年度肿瘤学科进展
以字为媒,以言为镜
汇集和解读属于肿瘤学者的2020
第1期

吉林省肿瘤医院 程颖教授
2020年度小细胞肺癌内科治疗领域进展
特邀专家

盘点2020之小细胞肺癌
小细胞肺癌作为难治顽固的恶性肿瘤,治疗进展非常缓慢,中位的生存时间停滞在10个月左右,5年的生存率不足7%,随着对SCLC分子机制认识的深入,新的药物不断涌现,SCLC领域也出现了突破性进展。
2018年凭借CheckMate032研究nivoluamb改写了SCLC三线及后线治疗无标准治疗选择的历史,2018年Impower133研究结果公布,广泛期SCLC迎来30多年来一线系统治疗中首个获得OS改善的3期研究,2019年FDA批准atezolizumab联合EC方案作为广泛期SCLC新的一线治疗标准,成为SCLC治疗史上新的里程碑;同年,中国研究者在SCLC治疗史上也写下浓重的一笔,我国自主研发的小分子多靶点抗血管药物安罗替尼在与安慰剂对照的经至少2种方案治疗的复发SCLC的2期研究中获得PFS和OS的双重获益,成为首个中国SCLC标准三线治疗选择,也开启了小分子多靶点药物在SCLC的研究热潮。转眼来到2020年,SCLC内科治疗领域依旧星光熠熠。这一年中国拥有了第一部独立的SCLC诊疗指南,让中国的SCLC规范诊疗日臸完善;首个SCLC免疫治疗在中国获批上市,实现了中国SCLC的治疗与国际同步;新的化疗药物鲁比卡丁获得FDA加速审批二线治疗SCLC以及小分子抗血管药物联合免疫治疗在复发SCLC的探索,让克服SCLC耐药燃起希望;免疫治疗前移局限期SCLC的研究让我们看到重新建立局限期SCLC治疗格局的号角已经吹响,而SCLC分子分型的深入研究将SCLC精准治疗的序幕徐徐拉开。1
中国首部独立的SCLC诊疗指南发布
2016年中国临床肿瘤学会(CSCO)基于医疗资源的不均衡性,兼顾循证医学证据以药物的可及性,颁布了首部适合我国国情的CSCO原发性肺癌诊疗临床指南。当时 SCLC仅作为原发性肺癌诊疗指南的一部。随着免疫治疗、抗血管靶向药物以及新型的化疗药物在SCLC领域不断突破,对转化性SCLC、神经内分泌肿瘤、复合型SCLC、副肿瘤综合征等认知的不断深入,以及中国研究者在SCLC领域进行的一系列研究结果公布,临床中迫切需要SCLC指南的内容变得更加全面、系统,为了让人们更了解SCLC,更加重视SCLC的研究,开展更深层次的探索,2020年在中国临床肿瘤学会指南工作委员会的指导下,CSCO小细胞肺癌专委会组织全国SCLC领域的权威专家重新编写了SCLC的诊疗指南,并且首次从原发性肺癌指南分离出来作为独立的指南出版发布。
第一部独立的小细胞肺癌CSCO指南充分考虑了我国患者的治疗意愿和需求,并参考国家医保目录,为患者制定更有效、更经济的治疗策略;同时指南依据中国主导的临床研究:ALTER1202研究、洛铂III期研究,中国参与的改变SCLC临床实践的国际临床研究:IMpower133研究、CASPIAN研究,充分体现出“中国制造和中国特色”,既彰显了我国研究者和企业研究能力、创新能力的提升,也体现了国际SCLC治疗的发展趋势;指南内容以表格+文字注释的形式体现,并附有用药剂量和方法、佐证文献、附录等,涵盖从SCLC的诊断、治疗到随访,尤其新增了SCLC的MDT诊疗模式、分子标志物,特殊SCLC(复合型SCLC、支气管肺/胸腺神经内分泌肿瘤和转化性SCLC)的治疗,以及放疗并发症的处理、副瘤综合征的治疗,文字简练、通俗易懂、便于查阅和携带,已经成为临床医生非常喜欢的“实用口袋书”,是目前中国首部、最专业、权威的小细胞肺癌诊疗指南。

2
中国首个SCLC免疫治疗药物上市
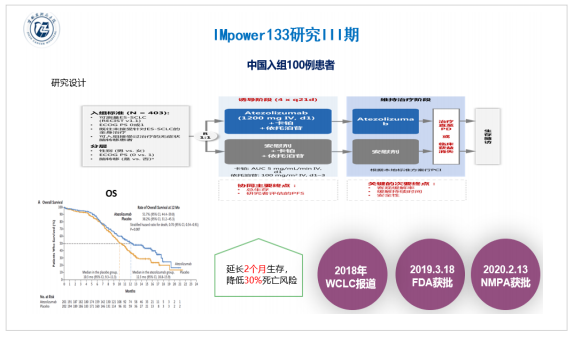
2018年世界肺癌大会上公布了来自SCLC领域的重磅研究—IMpower133研究,研究证实与标准化疗相比,atezolizumab联合化疗让广泛期SCLC的OS延长2个月,突破传统EP/EC方案的中位OS只有8-10个月的限制,降低30%死亡风险,同时也看到PFS的改善,Impower133研究成为30余年来在广泛期SCLC系统治疗中首个获得OS改善的随机对照3期研究,建立广泛期SCLC一线治疗的新标准,改写了SCLC的治疗史,成为SCLC的里程碑研究。根据这一结果2019年3月FDA获批atezolizumab联合化疗一线治疗广泛期SCLC。
在今年AACR会议上公布了更新的数据,IMpower133研究经过22.9个月的中位随访,与化疗相比,atezolizumab联合化疗依然保持了中位OS的优势。这项研究中国也贡献了100例患者广泛期SCLC患者,在FDA批准不到1年时间,2020年2月NMPA也批准了atezolizumab联合卡铂/依托泊苷一线治疗广泛期SCLC的适应症,这让atezolizumab成为第一个在中国上市的治疗SCLC的免疫药物,让免疫治疗真正惠及中国SCLC患者。根据IMpower133研究的结果以及NMPA的上市许可,CSCO小细胞肺癌诊疗指南2020版将atezolizumab联合依托泊苷/卡铂作为ES-SCLC一线治疗的I级推荐(1A类证据)。
3
FDA加速批准鲁比卡丁SCLC二线治疗
今年SCLC领域另一重要进展是二线治疗。自1998年拓扑替康获得SCLC二线治疗的适应症以来,一直没有新药获批。鲁比卡丁作为一种新的化疗药物,是海鞘素的衍生物,作为RNA聚合酶II的抑制剂,鲁比卡丁诱导DNA双链断裂和调节肿瘤微环境,在铂类耐药细胞和SCLC移植瘤模型中观察到很好的抗肿瘤活性。今年6月鲁比卡丁凭借一项多中心2期篮子研究的结果获得FDA加速批准用于治疗铂类药物化疗后疾病进展的转移性SCLC。在这项研究中一共纳入了105例SCLC,鲁比卡丁的ORR为35.2%,PFS:3.5个月,OS:9.3个月,进一步的分析中纳入的20例无化疗间歇(CTFI)≥180天的患者,鲁比卡丁单药治疗的ORR为60%,OS达到16.2个月,对于适合铂类再治疗的SCLC患者,鲁比卡丁略优于既往铂类再治疗的疗效,毒性相当,提示鲁比卡丁是敏感复发SCLC铂类再治疗的一种替代选择。根据这项研究结果NCCN 2021V1版的SCLC指南将鲁比卡丁作为复发SCLC(<6个月和≥6个月)的治疗选择,为2A类推荐。
然而最近Jazz Pharmaceuticals官网透露鲁比卡丁联合吡柔比星与CAV或者拓扑替康对比二线治疗SCLC的3期ATLANTIS研究没有达到主要研究终点,再次验证了SCLC二线治疗的探索之路崎岖不平,寻找SCLC复发耐药的机制,给予针对性治疗才能让改变SCLC二线治疗的窘局面。
4
小分子抗血管药物助力复发SCLC治疗
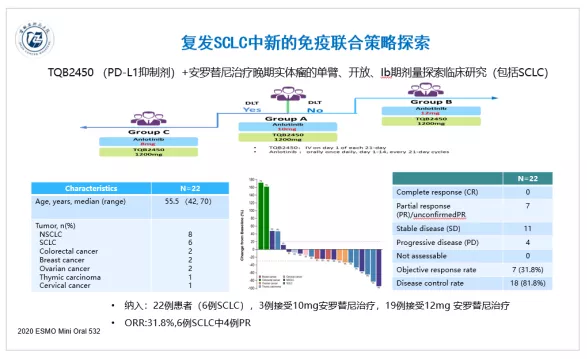
随着安罗替尼为SCLC三线及后线治疗带来PFS和OS的获益,成为中国SCLC三线及后线治疗选择以来,小分子多靶点抗血管药物已经成为SCLC领域研究的热点。今年小分子多靶点抗血管药物联合免疫治疗的研究在复发SCLC领域再传捷报。卡瑞利珠单抗联合阿帕替尼二线治疗广泛期SCLC的多中心、两阶段2期研究发现抗血管药物联合免疫治疗在铂类治疗复发的SCLC具有非常良好的抗肿瘤活性,而且敏感复发和耐药复发患者均可获益,同时联合治疗的毒性可以接受。无独有偶,安罗替尼联合PD-L1抑制剂TQB2450治疗晚期实体瘤的Ib期研究中纳入了6例SCLC患者,4例获得PR。提示免疫联合抗血管治疗是复发小细胞肺癌充满前景的治疗策略。
5
免疫治疗开启局限期SCLC探索
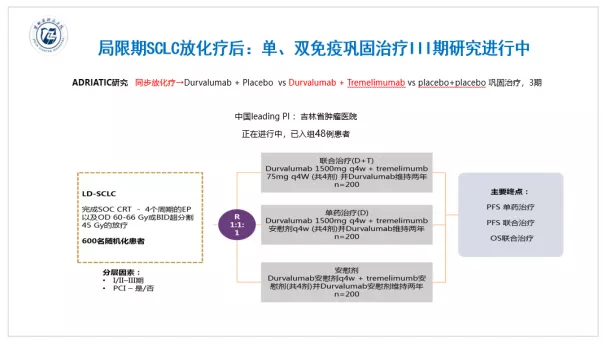
同步或者序贯放化疗自上个世纪80年代成为局限期SCLC的标准治疗模式以来,已经有30余年未曾改变了。随着免疫治疗为广泛期SCLC一线治疗和SCLC后治疗建立新的标准,研究者将改善局限期SCLC治疗现状的希望寄于免疫治疗。今年ESMO会议上公布了一项局限期SCLC放化疗后采用Nivolumab联合Ipilimumab双免疫巩固治疗的2期研究,发现诱导放化疗后Nivolumab+Ipilimumab巩固治疗并没有获得PFS 和OS的显著改善。由于这项研究开展较早,研究选择了毒性较大的方案(Nivolumab 1 +Ipilimumab 3),AE和因AE导致治疗终止的患者较观察组明显增加,这可能是影响免疫治疗发挥疗效的因素之一。ADRIATIC研究是同步放化疗后Durvalumab联合安慰剂或者Durvalumab 联合 Tremelimumab与安慰剂巩固治疗局限期SCLC的国际多中心的3期研究,目前这项研究正在招募入组中。另外,新型免疫药物TIGIT抑制剂联合atezolizumab巩固治疗局限期SCLC的II期研究也即将启航。
除了标准放化疗后免疫巩固维持的治疗模式外,免疫治疗从诱导治疗开始介入局限期SCLC的探索也已经开始。Pembrolizumab 联合同步放化疗治疗局限期SCLC的单臂单中心I/II期研究中,同步放化疗中加入免疫治疗具有良好的耐受性,初步的结果看到了良好的疗效,这项研究为后续开展随机对照研究提供了数据。目前免疫治疗在局限期SCLC的探索将为我们阐释局限期SCLC的免疫治疗如何进行更有效,更安全,这些研究可能成为未来改变局限期SCLC治疗格局的基础。
6
SCLC分子分型新探索
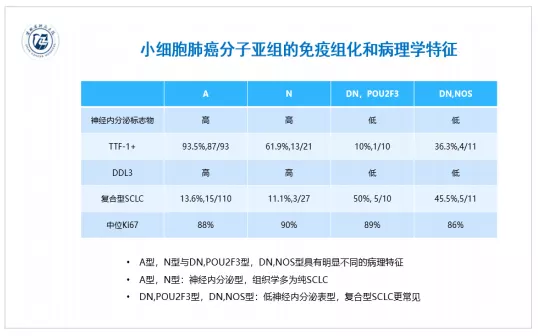
2019年Rudin教授提出根据4个关键的转录因子表达差异将SCLC分为A/N/P/Y四种亚类的设想,让我们对改善目前SCLC作为同质性疾病治疗的现状充满憧憬。研究者也陆续开展了针对SCLC分子分析的深入探讨。最近研究者通过对174 例SCLC的分析发现,ASCL1 和 POU2F3阳性的SCLC 患者ASCL1和POU2F3 的IHC通常多为高表达,在NEUROD1阳性SCLC中NEUROD1的IHC的表达范围宽度最大,YAP1阳性的SCLC中YAP1 的IHC通常低表达;根据SCLC中A、N、P、Y免疫组化表达情况,SCLC可分为A+,N+,A/N双阴P+(DN,POU2F3),双阴非特指型(DN,NOS),其中A/N双阳:37%, A/N双阴:14%,仅A阳:78%,仅N阳:45%,一般POU2F3专一的表达在ASCL-1和NEUROD1双阴性的肿瘤中,YAP1在各种亚型中都有表达,在A,N双阴的肿瘤表达更高;A型,N型通常为神经内分泌型,组织学多为纯SCLC;DN,POU2F3型和DN,NOS型SCLC通常为低神经内分泌表型,复合型SCLC更常见。可见A型,N型与DN,POU2F3型,DN,NOS型具有明显不同的病理特征,不同SCLC亚型治疗策略存在差异。
总结与展望
2020年SCLC继续前行,中国拥有了首部专门针对SCLC的诊疗指南,更加全面、系统的对SCLC进行了充分、系统的阐述和诊疗推荐,对于我国SCLC的规范化诊疗及新药研发都起到了积极的推动作用。Atezolizumab联合化疗获得NMPA批准一线治疗广泛期SCLC,实现了SCLC里程碑式的跨越,打破了三十年治疗无突破的窘境,免疫治疗真正惠及中国SCLC患者,在局限期SCLC中免疫治疗能否再下一城值得期待。鲁比卡丁虽然获得FDA加速批准二线治疗SCLC,但新的结果看到复发SCLC的治疗在曲折前行,免疫治疗联合小分子抗血管生成药物治疗的研究让我们看到了希望,而对分子分型和分子机制的深入理解才能SCLC真正走出困境,构建高效的新格局。
更多【盘点2020】,敬请期待!