中国抗癌协会
立即下载AppR+X治疗模式下,如何保持淋巴瘤患者的治疗强度?
抗肿瘤治疗过程中,维持适当的相对剂量强度(RDI)至关重要。然而,众多弥漫性大B细胞淋巴瘤(DLBCL)患者年老体弱、伴有若干合并症,这通常导致药物减量甚至停药。目前DLBCL患者接受利妥昔单抗+环磷酰胺+多柔比星+长春新碱+泼尼松龙(R-CHOP)方案治疗的中位RDI为58.9~87.9%1,变化范围较大,可见即使在新型治疗的背景下,DLBCL患者治疗强度降低的现象也较为突出,值得关注。
那RDI降低会对DLBCL患者造成那些影响呢?RDI的降低主要影响患者的生存状况。
透过多变量分析,我们发现RDI<70%与患者5年OS率(HR 9.61,p=0.006)2、2年OS率(OR 9.001,p=0.002)和PFS率(OR 2.599,p=0.007)降低3均显著相关。
值得注意的是,RDI降低可由抗肿瘤治疗过程中不良反应(AE)引发,其中较为常见的就是血液学相关AE,并以中性粒细胞减少为代表。一般来说,中性粒细胞减少是化疗常见的血液学不良事件和剂量限制性不良反应,可引起中性粒细胞减少性发热(FN),导致药物减量或治疗延迟,甚至会危及生命4。此外,DLBCL经典的R-CHOP方案中使用的利妥昔单抗也可能会引起中性粒细胞减少5。
目前,国内外多部权威指南、专家共识均推荐聚乙二醇化重组人粒细胞集落刺激因子(PEG-rhG-CSF)用于中性粒细胞减少的防治4,6-8。已有充足的临床证据显示,通过预防性使用G-CSF(包括PEG-rhG-CSF)可以降低包括淋巴瘤在内的等多种肿瘤患者FN的发生率,改善患者按期进行全剂量强度化疗的情况4。
日本就有学者探索了PEG-rhG-CSF用于接受R-CHOP方案治疗的DLBCL患者的作用。研究以PEG-rhG-CSF在日本获批的时间(2014年11月)为界,将患者分为2组:获批前组(n=209,抗肿瘤治疗始于2014年10月前)和获批后组(n=125,抗肿瘤治疗始于2014年11月后)。在获批前组中,仅6.2%(13例)患者每日使用G-CSF,多数患者于首次中性粒细胞减少时开始接受短效G-CSF治疗并于后续治疗周期中继续使用。在获批后组中,无患者使用短效G-CSF,76.8%(96例)患者于R-CHOP治疗期间至少使用一次PEG-rhG-CSF9。与获批前组相比,获批后组的RDI显著更高(86.8% vs. 67.8%,p<0.001,见图1A)。按照年龄将患者分为3个亚组(≤69岁、70~79岁、≥80岁)时,结论与之相似(见图1B),说明使用PEG-rhG-CSF的对各个年龄段的患者均具有维持RDI的作用9。
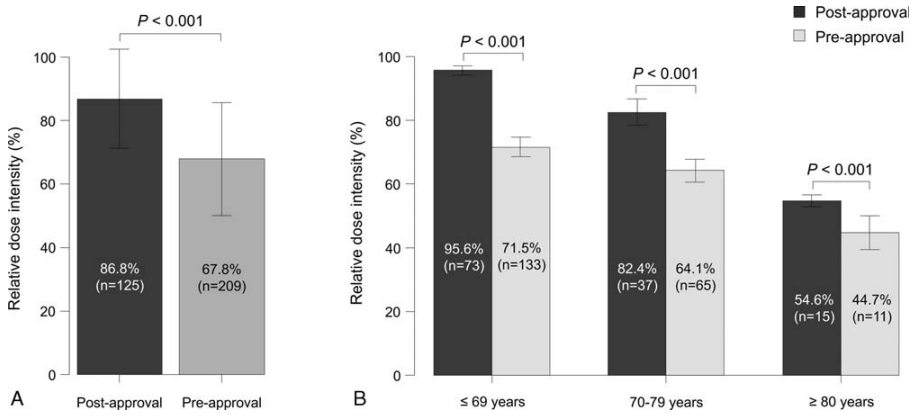
图1. (A)所有患者和(B)3个年龄亚组的患者中,获批前组和获批后组的RDI
多变量分析结果显示,患者纳入获批后组与RDI≥85%显著相关(OR 15.3,p<0.001,见表1)9。
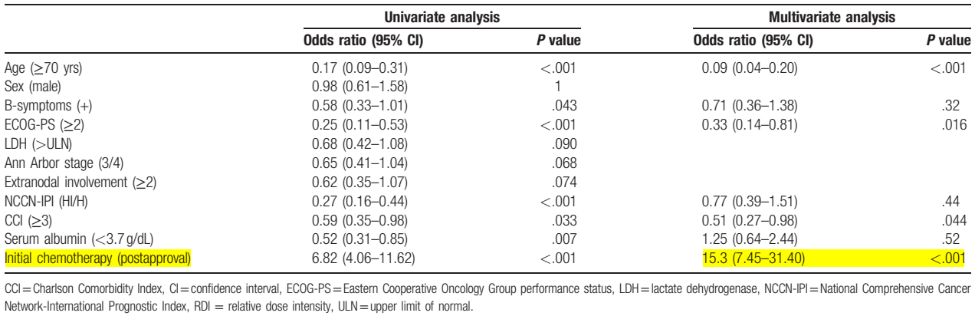
表1. RDI≥85%与各临床因素相关性的单变量和多变量分析
与获批前组相比,获批后组的FN发生率显著更低(20% vs. 38.3%,p<0.001),5年OS率和PFS率显著更高(OS率:85.7% vs. 69.9%,p=0.009;PFS率:81.4% vs. 64.4%,p=0.011;见图2A)。在美国国立综合癌症网络国际预后指数(NCCN-IPI)评分匹配的配对分析中,差异未体现出显著性(5年OS率:85.7% vs. 73.2%,p=0.091;5年PFS率:81.8%vs. 68.5%,p=0.12;见图2B)9。
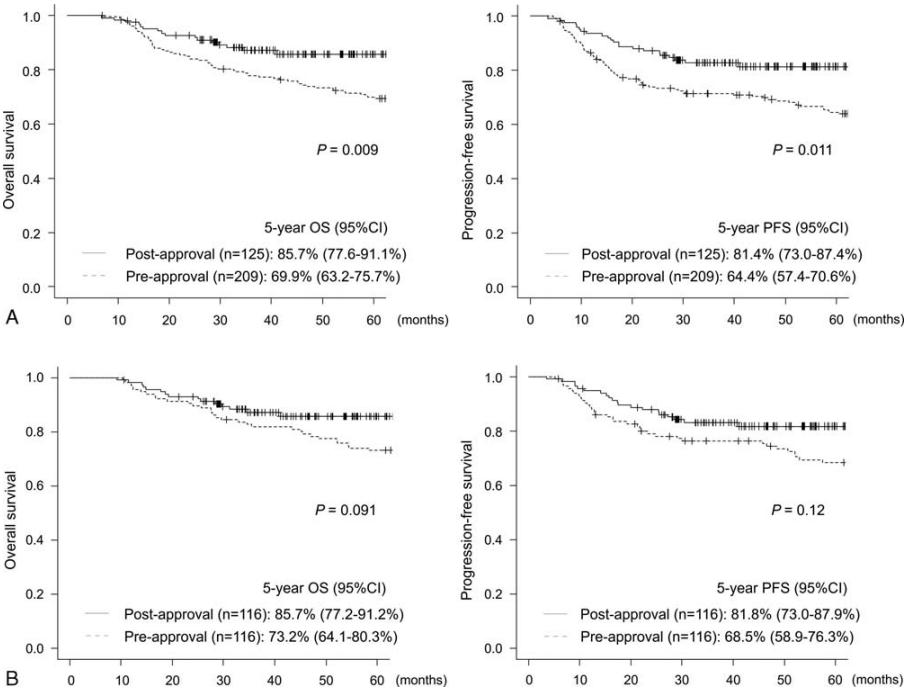
图2. (A)所有患者和(B)NCCN-IPI评分匹配的患者OS和PFS的Kaplan-Meier曲线
然而,在Ann Arbor 3/4期的患者(5年OS率:83.7% vs. 61.3%,p=0.019;5年PFS率:75.2% vs. 55.8%,p=0.034;见图3)、和NCCN-IPI高危的患者(5年OS率:80.7% vs. 32.4%,p=0.014;5年PFS率:75.6% vs. 27.5%,p=0.01;见图4)中也观察到了显著差异9。
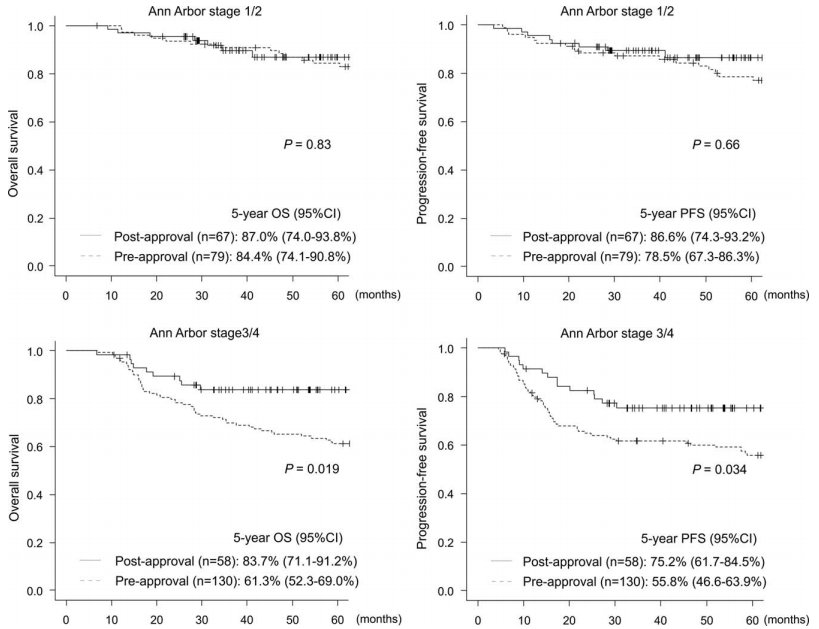
图3. 不同Ann Arbor分期患者OS和PFS的Kaplan-Meier曲线
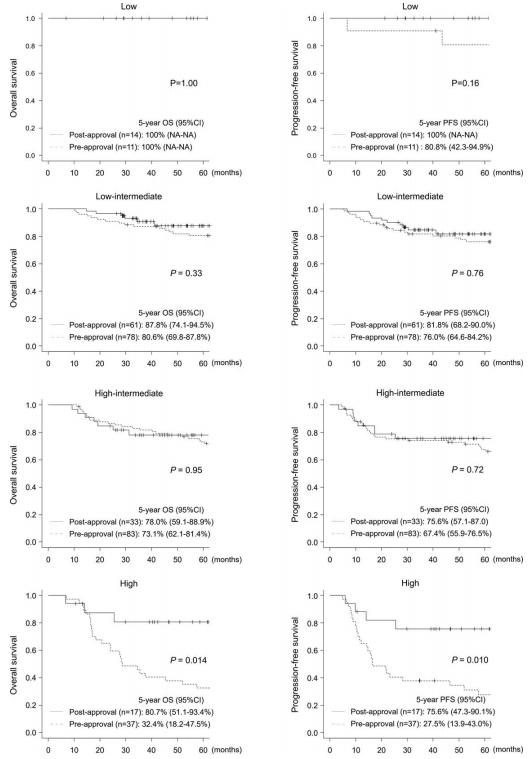
图4. 不同NCCN-IPI风险分层患者OS和PFS的Kaplan-Meier曲线
多变量分析结果显示,RDI≥85%与OS的改善相关(HR 0.48,95% CI 0.27~0.87,p=0.016)。PEG-rhG-CSF的使用,与OS的相关性,仅在单变量回归分析中得到证实(HR 0.52,95% CI 0.33~0.81,p=0.009,见表2)9。
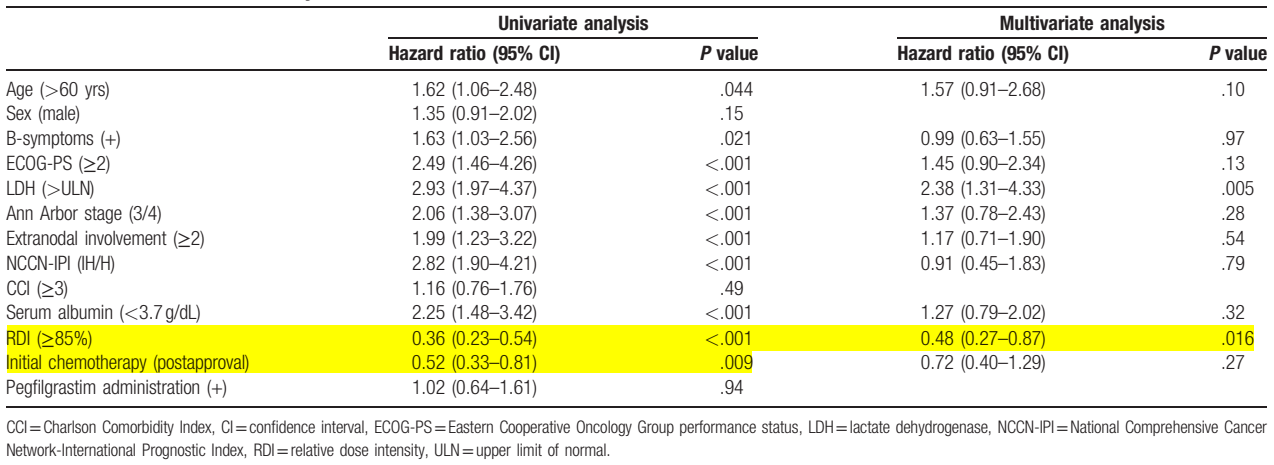
表2. OS与各临床因素相关性的单变量和多变量分析
尽管目前尚无研究直接证实PEG-rhG-CSF使用能够延长肿瘤患者的OS,然而,G-CSF的使用的确与抗肿瘤药物高RDI的维持相关10。此外,相较于短效G-CSF,PEG-rhG-CSF作为长效G-CSF有改善老年DLBCL患者PFS和OS的趋势,尽管差异并不显著11。
本研究首次证实了PEG-rhG-CSF使用与接受新型治疗(靶向治疗、免疫治疗)的肿瘤患者患者生存之间可能存在相关性,显示随着PEG-rhG-CSF投入使用,肿瘤患者的FN发生率下降、RDI增加,高危患者的PFS和OS显著改善。在获批后组中,进展期DLBCL或NCCN-IPI中-高危、高危患者更少,这可能是PEG-rhG-CSF的使用对总体OS或PFS无显著影响的原因。然而,值得注意的是,在临床高危患者中,维持高RDI能够显著改善OS。因此可以认为,后续值得开展研究继续探索PEG-rhG-CSF在低危患者中改善生存的作用。
既往众多研究均体现PEG-rhG-CSF用于恶性肿瘤患者能够有效提升绝对中性粒细胞计数(ANC)、降低中性粒细胞减少的发生率及缩短其时间、维持抗肿瘤治疗强度,基于此,培非格司亭、硫培非格司亭、拓培非格司亭等一系列PEG-rhG-CSF获美国食品药品监督管理局(FDA)、国家药品监督管理局(NMPA)批准上市,并在临床实践中接连取得了不俗的成绩。精准医疗时代下,希望后续能够开展的PEG-rhG-CSF相关研究更多、纳入的患者样本量更大以及来自各个风险分层的占比更均衡,这样才能够更清楚地探索PEG-rhG-CSF与患者预后的关系。
参考文献:
1. Bataillard EJ, Cheah CY, Maurer MJ, et al. Impact of R-CHOP dose intensity on survival outcomes in diffuse large B-cell lymphoma: a systematic review. Blood Adv. 2021 May 11;5(9):2426-2437.
2. Kanemasa Y, Shimoyama T, Sasaki Y, et al. The impacts of initial and relative dose intensity of R-CHOP on outcomes of elderly patients with diffuse large B-cell lymphoma. Leuk Lymphoma. 2017 Mar;58(3):736-739.
3. Hirakawa T, Yamaguchi H, Yokose N, et al. Importance of maintaining the relative dose intensity of CHOP-like regimens combined with rituximab in patients with diffuse large B-cell lymphoma. Ann Hematol. 2010 Sep;89(9):897-904.
4. 中国抗癌协会肿瘤临床化疗专业委员会,中国抗癌协会肿瘤支持治疗专业委员会. 肿瘤化疗导致的中性粒细胞减少诊治中国专家共识(2023版)[J]. 中华肿瘤杂志,2023,45(7):575-583.
5. 利妥昔单抗注射液说明书. 修改日期:2023年05月13日.
6. 中国医师协会放射肿瘤治疗医师分会,中华医学会放射肿瘤治疗学分会,中国抗癌协会肿瘤放射治疗专业委员会. 同步放化疗期间应用聚乙二醇化重组人粒细胞刺激因子中国专家共识(2023版)[J]. 国际肿瘤学杂志,2023,50(4):193-201.
7. 中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)肿瘤放化疗相关中性粒细胞减少症规范化管理指南(2021)[J]. 临床肿瘤学杂志,2021,26(7):638-648.
8. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®): Hematopoietic Growth Factors (Version 1.2024 — October 19, 2023).
9. Morita Y, Kanemasa Y, Sasaki Y, et al. Impact of pegfilgrastim approval on relative dose intensity and outcomes of R-CHOP for diffuse large B-cell lymphoma. Medicine (Baltimore). 2022 Mar 11;101(10):e29028.
10. Lyman GH, Dale DC, Friedberg J, et al. Incidence and predictors of low chemotherapy dose-intensity in aggressive non-Hodgkin's lymphoma: a nationwide study. J Clin Oncol. 2004 Nov 1;22(21):4302-11.
11. Ise M, Matsuda K, Shimura A, et al. Primary prophylaxis with pegfilgrastim during the first cycle of R-CHOP to avoid reduction of dose intensity in elderly patients. Int J Hematol. 2021 Jun;113(6):823-831.
编辑转载:歆语健康