中国抗癌协会
立即下载App【第七期】易树华-华氏巨球蛋白血症/淋巴浆细胞淋巴瘤诊断与治疗
疫情期间,为了给临床医生精准触达优质医疗资源,提升临床工作者规范化诊疗经验,由中国抗癌协会(CACA)血液肿瘤专业委员会、中国医学科学院血液病医院发起,CCMTV临床频道全程线上支持的“血液科专家在线教育讲座”栏目已经启动。第七期讲座由中国医学科学院血液病医院易树华老师带来【华氏巨球蛋白血症/淋巴浆细胞淋巴瘤诊断与治疗】的讲题,已经于 2020年3月23日上线,以下是针对此次精彩内容的回顾。
在讲解之前,让我们首先来看一个病例。患者男,64岁,首次就诊于2017年的1月,主诉发现球蛋白升高20余天,这是血液科淋巴瘤常见的主诉。血常规PLT 90*10⁹,血免疫球蛋白IgM 77.9g/L,血免疫固定电泳在γ区可见一条单克隆IgMκ成分,考虑单克隆IgM相关疾病。

在单克隆IgM相关疾病中,50%为MGUS,华氏巨球蛋白血症占17%,其他B细胞增殖性疾病、淋巴瘤、慢性淋巴细胞白血病、淀粉样变等也可导致IgM的升高,因此需要鉴别的疾病较多。今天我们主要讲解淋巴浆细胞淋巴瘤/华氏巨球蛋白血症(LPL/WM)。
2016年,由易树华教授、李剑教授、邱教授牵头,中国抗癌协会血液肿瘤专业委员会制定了《淋巴浆细胞淋巴瘤/华氏巨球蛋白血症诊断与治疗中国专家共识》。目前该专家共识的正在进行更新,可能在今年与大家见面。
LPL/WM的概念特征、诊断与鉴别诊断
LPL/WM的疾病定义
LPL/WM于1944年由Jan Gosta Waldenström首次报道并命名,2016年LPL的定义为由小B淋巴细胞、浆细胞样淋巴细胞和浆细胞组成的淋巴瘤,常常侵犯骨髓,也可侵犯淋巴结和脾脏,并且不符合其他可能伴浆细胞分化的小B淋巴细胞肿瘤的诊断标准。这里需要强调,首先定义中包含2~3类淋巴细胞,可以在形态学进行区分;其次这是排除性的诊断。当LPL侵犯骨髓同时伴单克隆IgM血症,则可诊断为WM。大约90~95%的LPL是WM,还有约10%的患者患者不分泌IgM,此时不能称其为WM,而应称为浆细胞淋巴瘤。早期报道显示在120例患者中有13%的患者是非IgM型,其中包括IgG,IgA及不分泌型。
WM诊断标准
因目前绝大多数LPL均为WM,故诊断和治疗标准的制定都是依据WM。WM的诊断标准依据的是2003年第二届国际巨球蛋白血症工作组的定义,并且尚未进行大的更改。WM诊断标准包括:①血液中检测到单克隆IgM(不论数量);②骨髓中浆细胞样或浆细胞分化的小淋巴细胞呈小梁间隙侵犯(不论数量);③免疫表型:CD5-, CD10-,CD25+, CD27+, FMC7+, CD79a+,CD103-, CD38/138+。10%-20%的病例可表达CD5、CD10或CD23,不能仅凭免疫表型排除WM;④ 除外其他已知类型的淋巴瘤;⑤ MYD88 L265P突变在 WM中的发生率高达 90%以上,但其阳性检出率与检测方法和标本中肿瘤细胞的比例等有关,肿瘤细胞比例需要占10%以上。由于WM患者肿瘤负荷本身较低,如不进行分选易出现假阴性。MYD88 L265P突变也可见于其他小B细胞淋巴瘤、弥漫大B 细胞淋巴瘤等。因此 MYD88 L265P 突变是 WM诊断及鉴别诊断的重要标志,但非特异性诊断指标。
WM临床表现
WM临床表现多种多样,总体可分为①肿瘤细胞直接浸润,侵犯骨髓导致血红蛋白、血小板和白细胞降低,侵犯淋巴结导致淋巴结/脾脏肿大,侵犯中枢神经系统导致Bing Neel综合症。②单克隆M蛋白血症,IgM分子较大,易导致高粘血症,出现鼻靵、头痛、视力障碍等;IgM是一种免疫球蛋白,易与自身组织反应导致免疫相关疾病,如IgM神经炎、冷球蛋白血症、冷凝集素病,以上表现也可导致患者乏力。
WM发病机制
① MYD88 L265P基因突变经磁珠分选后可出现于91%的WM患者,但不见于WM患者的正常组织和正常人B细胞,因此很少出现假阳性。少见于MZL、MALT及IgM型MGUS。MYD88 L265P基因可以通过IRAK4复合体向下传导信号通路,调节NFκB信号通路。MYD88 L265P上游为TLP受体,结合抗原后导致整个信号通路的活化。当MYD88 L265P突变后,可以募集磷酸化的BTK,直接活化下游信号通路而不需要上游信号的刺激,这是导致NFκB信号通路活化的重要因素,也是BTK抑制剂有效的原因。
② CXCR4基因突变与MYD88 L265P基因突变基本重叠,发生率约为30~40%。CXCR4突变后可以直接活化PI3K、AKT等信号通路,给细胞提供生长发育所需信号。因此CXCR4基因突变的患者可能影响BTK抑制剂的疗效。
诊断LPL/WM的常规检查项目
① M蛋白确定:进行免疫学检测,包括免疫球蛋白定量,血清蛋白电泳、血免疫固定电泳、24h尿蛋白定量。
② 病理学检查:因WM诊断必要条件是骨髓侵犯,故应进行骨髓活检、涂片、免疫组化和流式细胞术分析。如果有条件可以切除淋巴结进行活检、免疫组化及流式细胞术分析。针对MYD88 L265基因突变,最好在CD19磁珠分选后做二代测序,提高敏感性。
③ 影像学:需进行全身CT检查以评估全身淋巴结肿大。
④ 预后相关检查:WM的不良预后因素包括血清LDH水平升高、β2MG水平高、17P-/TP53突变、CXCR4突变等遗传学异常,目前CXCR4因比较复杂所以不作为常规检查。
⑤ 其他检查:包括眼底检查、血液粘滞度检查、直接抗人球蛋白实验和冷凝集素检测。如出现手指麻木等症状还需进行神经功能相关检查,怀疑周围神经病时可查抗MAG抗体和抗GM1抗体,但是这两项检查开展的单位不多,可能受到限制。
WM鉴别诊断
主要与IgM MGUS,MZL,IgM型骨髓瘤鉴别。
WM骨髓侵犯严重,淋巴结肿大较少,脾大及髓外侵犯相对比较少见,CD20表达水平较高,95%存在MYD88 L265P突变。IgM MGUS 有50%的可能性伴有MYD99 L265P突变,但没有其他情况出现。MZL骨髓侵犯较少,淋巴结肿大突出,特别是脾大在SMZL中比较常见,MALT常表现髓外侵犯,CD20高表达,MYD88 L265P突变率仅5%。IgM型骨髓瘤骨髓侵犯常见,但MYD88 L265P突变通常为阴性,同时常发生Cyclin D1或t(11;14)的遗传学异常,临床多发溶骨性改变,因此骨痛更为明显。
对该病例的后续病理学检查如下:
骨髓涂片:浆细胞比例增高(7.5%),淋巴细胞比例偏高(25.5%),并可见浆样淋巴细胞。
骨髓活检:少量异常浆细胞散在分布(约5%)。淋巴细胞散在或小灶性分布。网状纤维染色 (MF-0级)。
免疫组化:浆细胞为CD38+,CD138+,Kappa+,Lambda-,CD56-,CD20-。淋巴细胞为T、 B淋巴细胞混合增生,但B淋巴细胞数量偏多。
流式细胞分析:检测示可见两群异常细胞,一群细胞占3.77%,为单克隆B细胞。另一群异常细胞约1.5%,为单克隆浆细胞。
影像学检查:颈胸腹部CT未见肿大淋巴结,肝脾未见肿大。
所以该患者最终诊断为华氏巨球蛋白血症/淋巴浆细胞淋巴瘤

WM的治疗进展
无症状WM患者管理
淋巴浆细胞淋巴瘤总体上是一个惰性肿瘤,诊断时没有临床症状的患者通常以观察为主,WM同理。在西方国家有25%的WM患者是偶然被诊断的,在我国这一比例是6%,但随着体检的增多,门诊患者的比例也升高了。无症状患者应每3~6个月随访一次,进行查体、血常规、IgM变化水平等随访。
无症状WM进展的高危因素
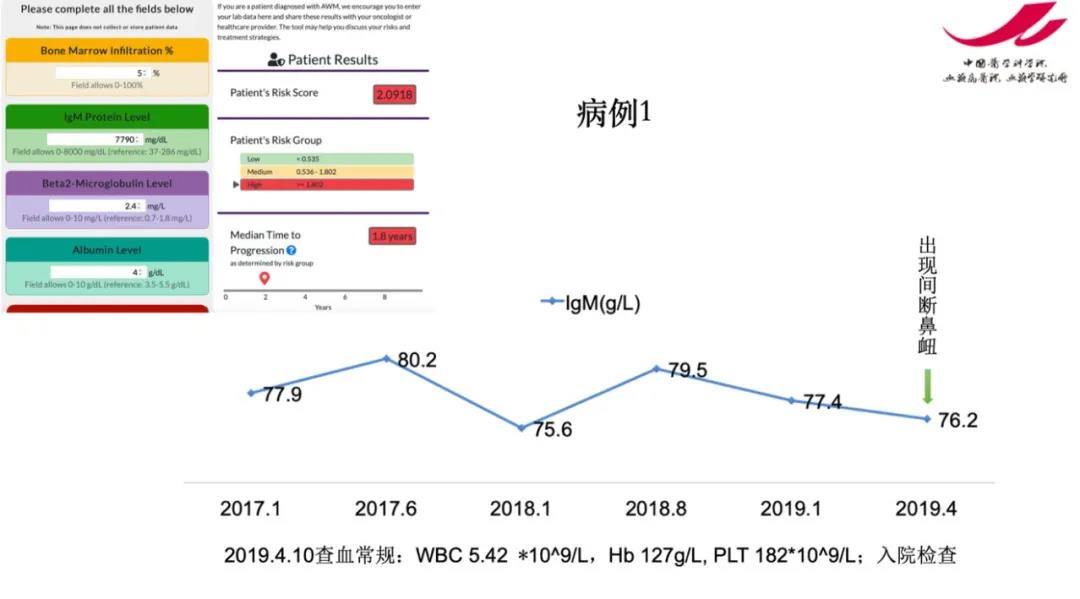
哈佛大学Dana-Farber癌症研究中心对此进行了长达23年的研究,中位随访7.8年,发现439名无症状WM患者中72%进展为有症状WM,28%仍不需进行治疗。对需要治疗的患者进行多因素分析发现,IgM≥4500,骨髓侵犯>70%,β2MG≥4,0mg/dL,白蛋白<3.5是独立的预后因素。据此他们在网站上做了一个预测模型,将患者分为低中高危三组,高危组在两年内进展至需要治疗,低危组经9年才进展至需要治疗,该模型经梅奥诊所及希腊的患者验证,预测价值较高。
例一中的患者经模型预测发现是高危型患者,从2017.1初诊至2019.4间断出现鼻靵症状,考虑与病情有关,IgM水平变化不明显,此时可以开始治疗。
 LPL/MM的治疗指征
LPL/MM的治疗指征
系统性症状:高热、没有原因的发热、盗汗、明显的体重减轻等;
症状性高黏滞血症,需进行血流变学的检查以判断是否需要治疗;
出现周围神经病变、器官肿大、淀粉样变、冷凝集素病、冷球蛋白血症、疾病相关的血细胞减少如血红蛋白、血小板的减少等症状;
髓外病变特别是出现中枢神经系统病变需治疗;
巨大淋巴结或有证据表明疾病转化时需及时治疗。
需要提醒的是单纯血清IgM水平升高不是本病的治疗指征;若血细胞减少是由自身免疫因素导致的,首选糖皮质激素治疗;若糖皮质激素治疗无效可针对原发病治疗。
WM的血浆置换治疗
对于高粘滞血症、IgM明显升高的患者首先要进行血浆置换缓解症状,经过2~3次每次约2000ml的置换后能使IgM下降30~60%。血浆置换术后应立即化疗,否则4~6周内IgM将恢复至原水平。
WM治疗演进
WM的药物治疗可以分为三个时代。在美罗华之前,以苯丁酸氮芥、CHOP、氟达拉滨±环磷酰胺方案为主的是传统化疗时代;利妥昔单抗及硼替佐米出现后进入新药治疗时代,疗效显著提高;2015年BTK抑制剂出现后进入靶向治疗时代,以口服治疗为主,包括BTK抑制剂伊布替尼、泽布替尼,BCL2抑制剂维奈托克,免疫抑制剂及小分子靶向药物等。
- 传统化疗时代
1.首先,R-CHOP方案为淋巴瘤治疗的经典方案,但不适合WM。根据R-CHOP,R-CVP和R-CP疗效比较的回顾性研究,三种方案疗效接近,R-CP方案疗效甚至更好,中性粒细胞缺乏性发热及治疗相关神经病发生率都显著降低。因此蒽环类药物和长春碱类药物在WM治疗中没有太多应用价值。
2.氟达拉滨多用于惰性淋巴瘤,在WM中治疗反应率可达70~90%,CR率<10%。但氟达拉滨骨髓抑制作用较重,存在持久性血细胞减少的风险,大细胞转化和第二肿瘤风险可能增加约10%,且会影响造血干细胞采集,因此对于年轻的或准备进行干细胞移植的患者用药需谨慎。
- 新药治疗时代
1.免疫调节剂国内可用的是沙利度胺和来那度胺,这是浆细胞骨髓瘤的常用药物,在WM治疗中也有效。特别是沙利度胺,在25例接受沙利度胺+利妥昔单抗治疗的患者中,总体反应率可达72%,主要反应率为64%。针对来那度胺的研究发现约81%的患者在治疗早期因红细胞下降而终止治疗,因此巨球蛋白血症患者应谨慎使用来那度胺,不作为常规推荐。
2.苯达莫斯汀+利妥昔单抗(BR)方案诱导治疗初治WM目前公布了两项临床试验的结果,StiL NHL1-2003试验对BR方案与R-CHOP方案进行了比较,BR方案ORR 92.7,CR 39.8%,PFS 69.5月,显著优于R-CHOP方案,5年OS 80.1%。StiL NHL7-2008试验探究了维持治疗的有效性,WM维持治疗ORR 91.4%,PR 89.9,中位PFS 78.0月,其中179例只接受BR的患者中位PFS 65.3月,结果与StiL NHL1-2003试验接近。
3.目前以硼替佐米/利妥昔单抗为主的方案主要包括BR、VR、RCD、VRD、IRD及CaRd方案等,ORR基本在90%左右,MRR也在70%以上。VRD方案中位PFS 42个月,三年持续反应率70%,3年OS 81%,效果也非常好;RCD方案两年PFS 67%,中位PFS 35个月也很好。
4.究竟哪个方案疗效较好的研究结果较少。梅奥诊所对BR和RCD方案进行了研究,结果显示初治患者BR和RCD方案有效率接近,BR方案深度缓解率更高;复发难治患者BR方案深度缓解率显著更高;BR组PFS和TTNT直观上优于DRC方案,但没有统计学差异。由于没有进医保之前利妥昔单抗和硼替佐米价格较高,我们对RCD方案和BCD方案疗效进行了对比,二者ORR接近,RCD方案的深度缓解率较高,PFS也优于BCD方案。因此利妥昔单抗是一个比较好的选择。
5.维持治疗是惰性淋巴瘤治疗不可避免的话题。Treon教授团队对利妥昔单抗维持进行了研究,诱导治疗方案比较多样,维持治疗方案也在2004年经历了变化。结果显示,利妥昔单抗维持的患者有41.8%疗效获得提高,而无利妥昔单抗维持的患者只有10%疗效提高。无论是初治还是复发的患者,维持治疗均可以显著提升PFS至一倍以上。另一研究表明WM患者接受BR诱导治疗后再进行利妥昔单抗维持获益不明显,可不进行维持治疗。
LPL/WM的新药
LPL/WM新药治疗是目前的趋势,但除BTK抑制剂和BCL2抑制剂外,其余新药距离临床应用还有一定距离。
1.伊布替尼是第一个BTK抑制剂,在一线二线治疗都有适应症,主要依据来自4个临床前瞻性研究,其中Pivotal试验纳入63例复发患者,INNOVOTE-1纳入31例复发患者,INNOVATE-2纳入了初治患者和复发患者,另一项Treon教授的研究纳入了30例初治患者。无论是初治还是复发的患者,伊布替尼有效率都非常高,在90%以上,初治患者可达100%;MRR均在70%以上,在初治患者中可达83%;VGPR率都不是特别高,在20%左右。Pivotal实验60个月的PFS达60%,INNOVATE-2试验30个月的PFS达82%。值得注意的是,去年Treon教授在lugano会议上更新的数据显示,伊布替尼的治疗反应及无进展生存均会受到MYD88和CXCR4突变的影响。MYD88及CXCR4均突变的患者较MYD88突变CXCR4野生型的患者ORR,MRR及CR率均降低;MYD88及CXCR4均为野生型的患者疗效更差,很少有患者能够达到MRR或VGPR,中位PFS仅5个月。63例患者总体的5年PFS 54%,5年OS 87%,单药伊布替尼与BR方案结果具有可比性。此外,Castillo教授在EHA上发布的研究结果显示,伊布替尼治疗的缓解深度与WM患者更好的PFS显著相关。
2.泽布替尼是第二个BTK抑制剂,ASPEN临床试验进行了队列一:复发/难治性或未经治疗的伴MYD88 L265P突变的WM患者和队列二:MYD88野生型患者这两个队列的研究,在去年12月公布了研究结果。队列一的结果显示泽布替尼较伊布替尼提高了MYD88突变型的WM患者治疗效果,但未达到统计学意义的差异。同时,泽布替尼较伊布替尼在安全性方面存在优势,3级及以上AE、因AE导致停药、致死性AE、房颤/房扑、高血压和轻微出血等不良反应比例均较低,中性粒细胞减少的比例较高,但肺炎发生率并没有提高。第二个队列显示,泽布替尼用于MYD88野生型的患者疗效较好,但后续还需进一步补充随访数据。
3.第三个新药是BCL2抑制剂维奈托克。哈佛大学主导进行了一项维奈托克治疗复发难治WM的II期临床试验,中位随访时间18个月,前期中位治疗2线,52%的患者前期接受过BTKi,结果ORR 达87%,MRR 81%,提示对于前期接受过BTKi治疗的患者,维奈托克也是很好的选择。
WM治疗推荐
由于WM较罕见,目前缺乏很好的横向对比研究,我们推荐对于WM患者首选参加设计良好的临床研究,其次优选的治疗方案包括BR、VRd、伊布替尼±R、RCD。其他的方案还包括苯达莫司汀单药、硼替佐米±R、泽布替尼单抗等。
LPL/WM治疗方案选择的注意事项
① 利妥昔单抗:存在燃瘤反应,应用初期可能导致IgM升高,加重高粘滞血症,故对于IgM高或伴有高粘滞血症的患者,不应单独应用或首先使用利妥昔单抗。
② 硼替佐米:可能加重外周神经病变,伴有外周神经病的患者应避免使用该类药物。硼替佐米可以快速降低IgM水平,可能会出现IgM水平很低但骨髓或外周血及外周淋巴结肿大效果不明显的不对称现象。
预后因素与疗效判断
WM的预后分层
1.国际ISSWM预后分层系统根据年龄>65岁、血红蛋白降低、血小板降低、β2MG明显升高及IgM水平明显升高五项危险因素,将患者分成了低危、中危、高危3组。但这一分期系统适用于传统治疗时代,在新药时代其效率有待研究。
2.对于中国的WM患者,ISSWM并不适用,主要原因是晚期患者比例较高。国内按照年龄>62岁、每>一系血细胞减少积一分的方式将患者分为3组,这一评估的效率较高。
3.去年欧洲提出了新的rIPSSWM评分系统,根据患者不同年龄段计分,将患者分为极低危到极高危共5组,曲线区分较明显,在未来的治疗中可能可以采纳。
4.TP53缺失/突变对WM生存的影响也很明显,2017年的研究显示TP53突变的患者,无论是初治还是复发难治的患者,预后均较差。对我国患者进行FISH检测及TP53分析,发现TP53缺失的患者预后同样较差。
WM的疗效判断标准
根据国际巨球蛋白血症工作组制定的疗效判断标准,以IgM水平为主要参考,两次免疫固定电泳阴性可判断为CR,M蛋白下降≥90%为VGPR,50~90%为PR,25~50%为MR,<25%为SD,两次检查M蛋白增加≥25%为PD。
在疗效判断时应注意:
① 血IgM定量受治疗的影响,利妥昔单抗IgM可能出现反弹并持续一段时间;
② WM起效相对缓慢,通常在3个月以上,硼替佐米和BTK抑制剂在2月左右,因此不必急于判断疗效;
③ 多数患者治疗不能达到完全缓解,因此患者和医生不必由于治疗未达完全缓解而更换药物,治疗有效的患者完成既定疗程或达到平台期后即可结束治疗或进入维持治疗,不必更换二线方案或做更积极的处理。
WM相关研究介绍
中国医学科学院血液病医院(血液学研究所)目前已治疗了320例WM患者,同时与Dana-Farber癌症研究中心的Treon教授确立了合作意向,计划开展从临床试验到基础研究的全面合作。目前有3项针对初治WM患者的临床试验以及3个针对复发难治WM患者的新药临床试验。
患者及家属可以从专业的患者组织比如华氏巨球蛋白血症支持小组这里获取信息,也可以拨打医院的咨询电话或在好大夫网站进行网上咨询。我们也将隔月组织一次专题讲座,在每周或隔周的周五中午进行答疑。