中国抗癌协会
立即下载App【第四期】徐卫- DLBCL的诊断与治疗
疫情期间,为了给临床医生精准触达优质医疗资源,提升临床工作者规范化诊疗经验,由中国抗癌协会(CACA)血液肿瘤专业委员会、中国医学科学院血液病医院发起,CCMTV临床频道全程线上支持的“战疫情,守健康——血液科专家在线教育讲座”栏目已经启动。第四期讲座由江苏省人民医院徐卫教授带来【DLBCL的诊断与治疗】的讲题,已经于 2020年3月15日上线,以下是针对此次精彩内容的回顾。
疾病介绍
淋巴瘤是起源于淋巴系统的肿瘤,主要分为霍奇金淋巴瘤和非霍奇金淋巴瘤(NHL)。NHL分为多个亚型,成人NHL最常见的类型为弥漫性大B细胞淋巴瘤(DLBCL)和滤泡性淋巴瘤。[1]DLBCL是非霍奇金淋巴瘤的最常见类型,几乎占到50%。
DLBCL也可产生于人体其他部位,如肠道、骨骼甚至是大脑或脊髓。基因检测表明DLBCL有多个亚型,尽管这些亚型在显微镜下看起来是一样的。DLBCL的各个亚型似乎有不同的预后和治疗效果。[2]
[1]https://www.cancer.gov/types/lymphoma
DLBCL的精准诊断
DLBCL WHO分型update 2016
2016年,WHO对DLBCL的分型进行了一些更新,相较于2008年的版本有很多变化。在对DLBCL进行诊断时,主要分为非特指型和一些特殊亚型。对于非特指型DLBCL,新版的DLBCL分型中要求医务人员要掌握细胞起源。此外,还提出很多了特殊亚型,其中有些需要格外重视。比如富余T细胞亚型等,这些亚型的提出对患者后续的治疗选择很有意义,临床医生应该对这些亚型予以重视。
2008版分类中将“老年EBV阳性DLBCL”作为一个暂定亚类,但近年来认为,只要是EBV阳性的患者,预后都比较差,且与年龄无关,因此2016版分类将“老年”移除。但需要注意的是,2016分类将EBV阳性黏膜与皮肤溃疡从EBV阳性DLBCL中单独区分出来,这类型的患者的治疗效果是非常好的,甚至能达到治愈。
还有一种源发纵隔的大B细胞淋巴瘤也需要格外注意,如果诱导治疗方案得当,有些患者甚至都不需要放疗,也不需自提移植,5年生存率可达90%。
在高级别B细胞淋巴瘤分类中,也分为特指型与非特指型。特指型就是指,所有伴有MYC和BCL2和(或)BCL6重排的LBCL,也就是临床医生常说的“双打击”或“三打击”。
DLBCL的异质性非常大
众所周知,DLBCL的异质性非常大,可以说是“同病不同命”。不同的发病部位、不同的细胞起源、不同的IPI指数、不同的生物标志物都影响着DLBCL的治疗效果。目前,我们对DLBCL的认识还很局限,不过是冰山一角。
从基因突变的角度来看,DLBCL与传统血液肿瘤还是很不一样的。DLBCL的突变频率呈长尾特征,即使是最多见的突变也只影响大约10%~20%的患者,不同报道中重叠的基因只占约10%。
DLBCL分类的里程碑研究
根据新英格兰杂志刊登的一篇重磅报道,研究人员通过对372个基因进行分析,希望检出有重现性异常的基因。根据实验结果,研究人员将DLBCL分为四个亚型,分别为MCD型、N1型、BN2型和EZB型。MCD型有MYD88L265P和CD79B的突变,且绝大多数为ABC;BN2型有BCL6融合和NOTCH2突变;N1亚型有NOTCH1突变,且绝大多数为ABC;EZB型有EZH2突变和BCL2易位,绝大多数为GCB。研究还发现,EZB、BN2两种亚型的PFS和OS要优于MCD和N1。
无独有偶,Nature Medicine杂志上也发表了一篇关于DLBCL分型的研究,该研究分析了304例接受R-CHOPlike方案治疗的患者。根据实验结果,研究人员分为5种类型,分别为C1、C2、C3、C4和C5。C1型,表现为BCL6融合和NOTCH2突变,对应上文的BN2亚型;C2是有P53的突变;C3对应上文的EZB亚型;C5则对应MCD型。
DLBCL分型的进展
我们对DLBCL的分型就不能局限于细胞起源,因为这远远不能满足临床需求。随着对DLBCL的进一步认识,我们对于DLBCL的认识应该尽快发展到基因分型的阶段,并尽早投入到临床应用,这也会为更多患者带来希望,意义非常重大。
DLBCL的治疗
年轻患者的治疗
对于初治患者,治疗前需要对患者进行分组和分层。首先根据患者年龄进行分组,如果患者较为年轻(≤60岁),那么再根据aaIPI评分来分层,年轻患者的治疗方案如下表所示。
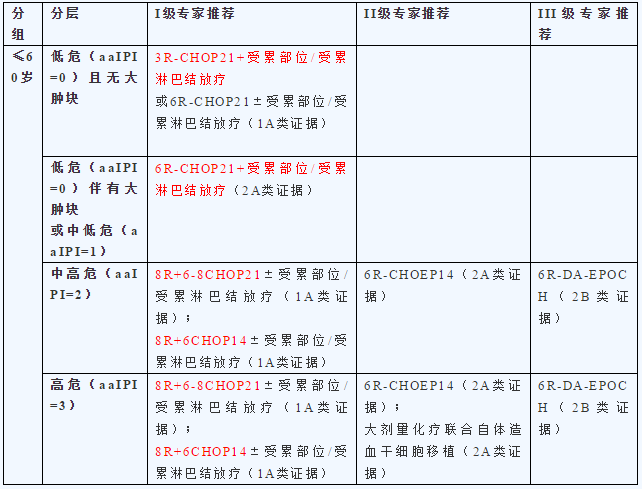
对于年轻高危或中高危的患者,参与临床试验仍是首选,因为对于这些患者,传统的8R联合6-8疗程的方案效果并不是特别好。化疗前大肿块或界外器官受侵、化疗后未达到CR的患者应进行放疗。自体干细胞移植可作为高危患者的巩固治疗的作用尚无定论,有研究显示,移植后的PFS有显著延长,但OS无差别,因此仍需进一步验证。对于双打击淋巴瘤患者,应采用强化疗方案,如R-HyperCVAD、R-DAEPOCH等。
高龄患者的治疗
在治疗DLBCL时,我们通常都会把蒽环药物作为一线治疗使用,而蒽环药物最大的缺点就是对心脏功能的影响。对于年龄较大的患者,他们的身体状态往往较差。因此,在治疗年龄较大的患者时,需要评价其心功能,治疗方案如下表所示。
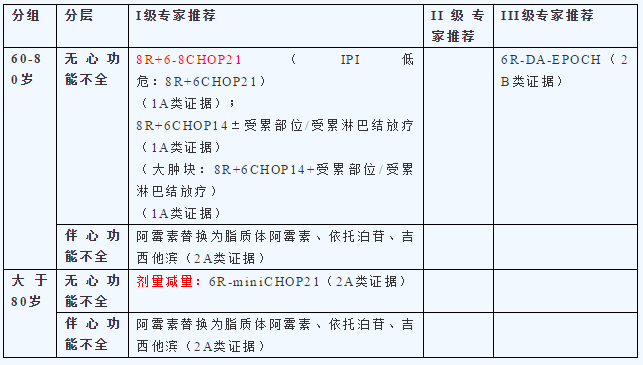
FLYER研究
6*R-CHOP方案是年轻DLBCL的标准疗法,有很好的效果。FLYER研究的研究目的是探索年轻DLBCL患者采用4*R-CHOP+2*R方案的治疗效果不劣于标准治疗且毒性降低。FLYER研究入组的患者均为年轻的轻症患者,这些患者非常早期,中位随访33个月。根据试验结果来看,试验组(4*R-CHOP+2*R)三年的EFS、FPS和OS都与试验组(标准治疗组)相当,没有显著性差异。在治疗效果不变的基础上,试验组的不良事件发生率明显下降。这个研究很值得推荐,年轻轻症患者可能会因此获益。
GOYA研究
那么对于初治患者,CHOP应该用6个周期还是8个周期呢?根据GOYA研究中的R-CHOP组设置了两种方案,分别为8R+6CHOP和8R-CHOP,并评估了两者的PFS、OS和不良事件情况,中位随访3.9年。根据试验结果来看,两者的PFS相当,CHOP6组的OS甚至更高一些,可见减少了2周期CHOP并不影响治疗效果。亚组分析发现,CHOP8也并不会额外增加高危患者的PFS获益。还有一点需要注意,CHOP8要比CHOP6的不良事件发生率高得多。
DLBCL的治疗仍有提升空间
DLCBL是一种可以治愈的疾病,但仍有40%-50%患者,出现难治或复发的情况。如何更有效地治疗这部分病人,是现在面临的最大的挑战。近20年来,科研人员一直尝试去改进R-CHOP方案,但其一线治疗的地位始终没有被动摇。其中虽有两个有一定趋势的试验,但也没有取得实质性结果,接下来就跟大家分享一下这两个试验。
PHOENIX研究
PHOENIX是一项II期研究,试验组在R-CHOP加入了伊布替尼,对照组为R-CHOP+安慰剂。首要终点为ITT人群的EFS和ABC亚型的EFS,次要终点为PFS、CR、OS和安全性。试验结果发现,加入伊布替尼,对治疗效果没有任何影响。
在对本研究进行分析后发现,对于年轻患者(<60岁),R-CHOP联合伊布替尼可以明显地提高EFS和OS。研究还发现,R-CHOP联合伊布替尼的方案似乎让双表达的DCBCL患者的生存获益优于R-CHOP,尤其是对于60岁以下患者。研究人员表示,毫无疑问加入伊布替尼会增加毒副反应,但年轻患者身体条件较好,不会像老年患者那样出现较多的停药现象,这种停药现象会与伊布替尼的效果抵消。这也解释了为什么年轻患者中会有差异,而老年患者没有差异。
ROBUST研究及其他相关研究
ROBUST研究是一项III期研究,备受期待,但遗憾的是,试验结果为阴性。试验组的治疗方案是在R-CHOP的基础上加入来那度胺(R2-CHOP)。在入组试验前,必须做NanoString检测,对ABC人群进行随机,GCB患者无法入组,这需要花费1个月时间。从试验结果来看,R2-CHOP与对照组相比,主要研究终点PFS没有显著性差异,ORR和CR并无有意提高。试验的次要终点EFS也没有显著性差异,OS也没有显著性差异。试验人员认为,NanoString检测的等待时间过长,也是该试验失败的主要原因之一。
无独有偶,在梅奥诊所开展的E1412试验,试验组也是在R-CHOP的基础上加入来那度胺(但来那度胺的剂量不同),但该试验没有针对ABC进行入组,而是所有DLBCL患者都可参与。根据试验结果,该研究达到了主要研究终点,PFS出现显著差异,R2-CHOP,相比于R-CHOP的PFS更长,OS也有延长的趋势。普遍认为,E1412试验出现显著性变化的原因是没有过长的用药等待时间,入组患者中不全是ABC人群,以及用药剂量的不同。
还有一项名为HOVON多中心II期研究,评估R2-CHOP用于MYC重排DLBCL的疗效。试验的主要终点是PET-CT扫描评估的完全代谢缓解率(CMR)。PFS和OS均显著高于历史对照数据。
除上述的两个试验外,还有名为“SMART START”的试验,绝大多数入组病人都为晚期,治疗方案为利妥昔单抗+来那度胺+伊布替尼(RLI)方案联合CHOP。结果显示,未开始化疗时患者ORR达到86%,其中近36%的患者达到CR。随后,患者接受8个周期标准化疗后,ORR达到100%,CR率为95%,很有前景。当然,有前景的试验不止这些,这也进一步说明了医务人员加深对DCBCL认识的重要性。
老年患者的相关研究
80岁以上的患者,不能耐受强烈化疗。法国的GELA LNH03-7B研究的给药方案为R-miniCHOP21(CHOP几乎减半)。结果显示,对于体能较好的患者,R-miniCHOP21是一种安全有效的方案。江苏省人民医院另辟蹊径,将R-GemOx方案用于一线治疗。试验结果发现,R-GemOx方案对老年人群同样有效,三年OS还要优于法国的GELA LNH03-7B研究。
DLBCL的维持治疗
对于60岁以上的老年患者不适合接受移植,且预后就较差,如果在接受6到8个周期的R-CHOP治疗后就停止治疗,很容易复发。科研人员也在一直探索用什么样的方法来维持治疗,但始终没有很好的结果。在使用来那度胺的REMARC的研究中,观察到了PFS的显著延长,但OS没有显著差异。
复发难治患者的治疗
对于复发或难治患者的治疗方案如下表所示。
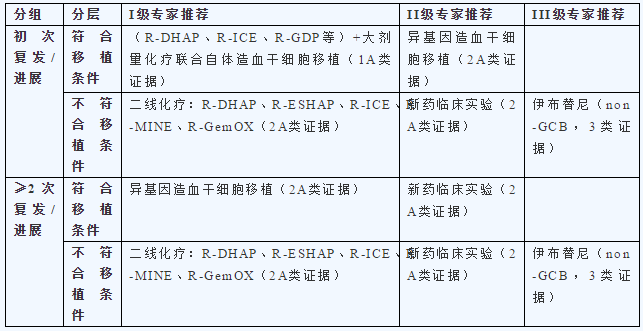
临床上有多种挽救方案,多为利妥普单抗联合化疗。但目前来说,未有明显数据表明某一种方案明显优于其他方案,因此总的来说,尚未出现最佳的挽救方案。对于自体移植后复发或挽救方案难治的患者,可考虑异基因移植。
CD79b免疫耦合剂Polatuzumab(PV)+BR的试验结果非常令人期待。根据该试验公布的结果,对于不适合移植的复发/难治DLBCL患者,接受PV联合BR方案可以获得更有效的缓解,PFS、DOR和OS都得到了极大改善,且安全可耐受。美国FDA也已批准Polatuzumab用于治疗复发或难治的DLBCL患者。
CAR-T也成为了复发/难治DLBCL患者的重要治疗手段,取得了很好的效果,也值得进一步探索。还有一点需要注意,我们不能盲目地“迷信”PD-1、PD-L1抑制剂,只要选择合适的DLBCL患者才会取得较好的疗效。
ctDNA液体活检在淋巴瘤诊疗中的应用
在初诊时,ctDNA液体活检可以检查DNA的突变和基因易位,可以帮助医务人员进行预后分层。在治疗和随访过程中,可以通过ctDNA液体活检,来进行患者的疗效监测。对于复发的情况,可以通过再次活检,帮助医务人员预测复发和耐药监测。可以说,ctDNA液体活检可以应用到淋巴瘤诊疗的任何一个阶段。ctDNA液体活检还可以克服空间的异质性,可以提早发现发生转化的情况,可应用于淋巴瘤精准诊疗的多个阶段,在DLBCL的精准诊疗中意义重大。
总结
DLBCL是一种异质性很强的疾病,随着NGS技术的发展,医务人员对淋巴瘤的不同亚型的分子分型更加准确,可以更全面地了解不同类型的淋巴瘤分子特征。虽然R-CHOP是DLBCL的一线有效治疗方案,但仍有接近一半的患者出现了复发或难治的情况,我们仍应从DLBCL的发病机制、分子机制等方面入手,进行新药新技术的开发与研究。在临床治疗中,医生应活用ctDNA液体活检技术,得益于该技术克服时空异质性的优点,可对淋巴瘤患者进行全程管理,精准诊疗。