中国抗癌协会
立即下载AppCell Res | 重大进展,浙江大学杨波/何俏军/马胜林发现烟酸可逆转索拉非尼诱导的手足皮肤反应,造福肿瘤患者
2020年4月15日,浙江大学杨波,何俏军及马胜林共同通讯在Cell Research 在线发表题为“s-HBEGF/SIRT1 circuit-dictated crosstalk between vascular endothelial cells and keratinocytes mediates sorafenib-induced hand–foot skin reaction that can be reversed by nicotinamide”的研究论文,该研究显示血管内皮细胞是索拉非尼诱导的HFSR的主要细胞靶标,其中可溶性肝素结合表皮生长因子(s-HBEGF)介导了血管内皮细胞与角质形成细胞之间的串扰。
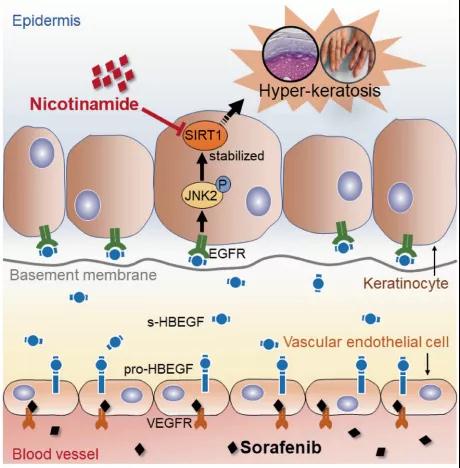
从机制上讲,从血管内皮细胞释放的s-HBEGF激活角质形成细胞上的表皮生长因子受体(EGFR)并促进c-Jun N末端激酶2(JNK2)的磷酸化,从而稳定了必需的角化蛋白诱导物sirtuin 1(SIRT1) ,最终产生了HFSR。体内施用s-HBEGF无需索拉非尼治疗即可充分诱导过度角化。此外,该研究报道了HBEGF中和抗体,Sirt1敲低和经典的SIRT1抑制剂烟酰胺都可以在小鼠模型中显著降低索拉非尼诱导的HFSR。值得注意的是,在一项初步临床研究中,烟酰胺的一种前药烟酸可实质上逆转索拉非尼诱导的HFSR。总的来说,该研究发现揭示了角质形成细胞中血管内皮细胞促进角质化的机制,并为索拉非尼诱导的HFSR提供了潜在的有前景的治疗策略。

索拉非尼是一种多激酶抑制剂,靶向与肿瘤进展和肿瘤血管生成有关的酪氨酸受体和丝氨酸/苏氨酸激酶。在许多国家/地区已被批准作为晚期肝细胞癌,转移性甲状腺癌及晚期肾细胞癌患者的一线治疗药物。对于大多数此类患者,索拉非尼是唯一产生良好治疗效果的药物。但是,它与手足皮肤反应(HFSR)的高发生率相关,阻碍了该抗癌药的临床应用。ClinicalTrial.gov和其他已发表论文的临床试验报告表明,索拉非尼诱导的HFSR的发病率范围为30%至高达76%。对于严重HFSR的患者,应降低剂量或需要中断治疗,这会降低索拉非尼的治疗效率,甚至无法缓解癌症的进展。
索拉非尼诱导的HFSR的特征是手掌和足底区域过度角化。过度角化,定义为角质层增厚,通常是由于角质形成细胞表皮稳态的异常所致,包括过度增殖和过度分化。大量研究发现,大多数药物诱导的皮肤毒性是直接影响角质形成细胞的途径的后遗症,因此,角质形成细胞功能障碍被广泛认为是索拉非尼的主要原因。
但是,基于这种概念的干预策略被证明是无效的。例如,通过预防性去除角化过度区域来控制足底角化过度的存在,然后应用保湿霜,对严重的HFSR(II级或III级)几乎没有影响。此外,HFSR患者几乎无法受益。因此,对于患有更严重的HFSR患者,必须减少剂量或中断剂量,这不可避免地限制了索拉非尼的治疗效果。迫切需要基于索拉非尼诱导的HFSR潜在机制,开发有效的干预措施。
血管内皮细胞的生长导致形成向皮肤细胞提供营养的血管。先前已经报道了血管内皮细胞和角质形成细胞之间发生串扰的情况。例如,紫外线B(UVB)可以诱导血管内皮细胞分泌一氧化氮(NO),从而促进DNA损伤及其邻近角质形成细胞的遗传转化。
在这项研究中,研究人员阐明了索拉非尼诱导的HFSR的机制。揭示了血管内皮细胞和角质形成细胞之间的串扰,其中从血管内皮细胞释放的s-HBEGF稳定了sirtuin 1(SIRT1),它是角质形成细胞中必不可少的角化诱导剂,并最终引起HFSR。基于这种机制的见解,研究人员进一步证明了HBEGF中和抗体和经典的SIRT1抑制剂烟酰胺可以逆转索拉非尼诱导的HFSR,因此为治疗这种毒性提供了潜在的有希望的治疗策略。
参考消息:
https://www.nature.com/articles/s41422-020-0309-6